奈玛特韦/利托那韦(Nirmatrelvir/ritonavir)是一种组合包装的用于治疗新冠病毒感染的抗病毒药物,属于复方口服制剂,是由150mg奈玛特韦片和100mg利托那韦片组成,未纳入医保。
本页面主要目录有关于奈玛特韦/利托那韦的:医学用途、药理机制、药代动力学、风险与禁忌、历史、临床数据、使用情况、化学信息、专利、争议、附表等介绍
奈玛特韦/利托那韦(Nirmatrelvir/ritonavir)是一种组合包装的用于治疗新冠病毒感染的抗病毒药物,属于复方口服制剂,是由150mg奈玛特韦片和100mg利托那韦片组成,未纳入医保。
本页面主要目录有关于奈玛特韦/利托那韦的:医学用途、药理机制、药代动力学、风险与禁忌、历史、临床数据、使用情况、化学信息、专利、争议、附表等介绍
奈玛特韦/利托那韦
Nirmatrelvir/ritonavir
帕罗韦德,Paxlovid
片剂
成人伴有进展为重症ND高风险因素的轻至中度新型冠状病毒感染(COVID-19)
口服
化学药品
未纳入医保
处方药
无
主要用于发病5天以内的轻至中型新型冠状病毒感染(COVID-19)且有进展为重症高风险因素的成人患者。
奈玛特韦可以阻止病毒复制,而利托那韦可以减缓奈玛特韦的代谢而提高其在体内的暴露水平,从而使奈玛特韦在体内的作用时间延长,并提高血药浓度,发挥药物的协同作用。
该药是肝药酶 (如CYP3A)和转运蛋白(P-gp、BCRP 和 OATP1B1)的抑制剂,与很多药物有药物相互作用,其中不得与高度依赖CYP3A进行清除的且其血药浓度增加可能导致严重甚至危及生命的不良反应的药物联用。
该药不良反应常见腹泻、味觉倒错等,偶见消化不良、呕吐、头晕、肌痛、转氨酶升高等。
结合奈玛特韦/利托那韦药品说明书及中国新型冠状病毒感染诊疗方案(试行第十版),该药主要适用于发病5天以内的轻、中型COVID-19且伴有进展为重症高风险因素的成年患者。
COVID-19重症高风险因素主要包括:
年龄大于65岁 ,尤其是未全程接种新冠病毒疫苗者;
有心脑血管疾病(含高血压)、慢性肺部疾病、糖尿病、慢性肝脏、肾脏疾病、肿瘤等基础疾病以及维持性透析患者;
免疫功能缺陷(如艾滋病患者、长期使用皮质类固醇或其他免疫抑制药物导致免疫功能减退状态);
肥胖(体质指数≥30kg/m);
晚期妊娠和围产期女性;
重度吸烟者。
注意奈玛特韦/利托那韦不用于无进展为重症的危险因素的有症状患者,或无症状的新型冠状病毒(SARS-CoV-2)感染者。
制剂
奈玛特韦/利托那韦是奈玛特韦片和利托那韦片组合包装,为复方制剂,剂型为片剂,未纳入医保。
规格
奈玛特韦片每片150mg,利托那韦片每片100mg。
用法
口服。可与食物同服,也可不与食物同服。片剂需整片吞服,不得咀嚼、掰开或压碎。
该药为奈玛特韦片与利托那韦片的组合包装。奈玛特韦必须与利托那韦同服。如不与利托那韦同服,奈玛特韦的血浆水平可能不足以达到所需的治疗效果。
用量
推荐剂量为奈玛特韦300mg(150mg×2片)联用利托那韦100mg(100mg×1片),一天给药2次,每12小时1次,连续服用5天。在COVID-19确诊及出现症状后5天内尽快服用。如果患者在开始使用该药治疗后因重症或危重COVID-19需要住院,也建议完成5天的治疗。
如果漏服一剂但没有超过通常服药时间的8小时,则应尽快补服并按照正常的给药方案继续用药。如果漏服且超过8小时,不应补服漏服的剂量,而应按照规定的时间服用下一剂量。请勿为弥补漏服的剂量而服用双倍剂量。
特殊人群
轻度肾功能损伤患者(eGFR≥60至90mL/min),无需调整剂量;
中度肾损伤患者(eGFR≥30至<60mL/min),将该药剂量减少至奈玛特韦/利托那韦150mg/100mg,每12小时1次,持续5天,以免过度暴露;
重度肾损伤患者(eGFR<30mL/min),不应使用该药,包括血液透析下的终末期肾病(ESRD)。
轻度(Child-Pugh A级)或中度(Child-Pugh B级)肝损伤患者,无需调整该药剂量;
重度肝损伤患者,不应使用该药。
奈玛特韦/利托那韦是奈玛特韦片和利托那韦片的组合制剂,其中奈玛特韦是一种SARS-CoV-2主要蛋白酶Mpro(也称3C-样蛋白酶,3CLpro)的拟肽类抑制剂,可以抑制SARS-CoV-2 Mpro,使其无法处理多蛋白前体,进而阻止病毒的复制。
此外,奈玛特韦还是细胞色素P4503A酶(CYP3A)的代谢底物,主要由CYP3A4代谢后失活,因此影响CYP3A代谢酶系统的药物会影响奈玛特韦的血药浓度,而利托那韦是CYP3A抑制剂,可以减缓奈玛特韦的代谢,从而提高其在体内的暴露水平,使奈玛特韦在体内的作用时间延长,并提高其血药浓度,发挥药物的协同作用。
已在健康受试者中开展了奈玛特韦/利托那韦的药代动力学研究。利托那韦为CYP3A4抑制剂,与奈玛特韦联用后可增加奈玛特韦全身暴露。
健康受试者单次空腹口服奈玛特韦混悬剂250mg后AUCinf、AUClast、Cmax的几何均值分别为3513ng•h/mL、3318ng•h/mL、883.1ng/mL,半衰期T1/2约为5.6h;单次口服奈玛特韦混悬剂/利托那韦片250mg/100mg后AUCinf、AUClast、Cmax的几何均值分别为28220ng•h/mL、27600ng•h/mL、2882ng/mL,半衰期T1/2约为6.9h(见附表1)。
健康受试者单次空腹口服奈玛特韦混悬剂/利托那韦片250mg/100mg~750mg/100mg,奈玛特韦暴露量增加比例小于剂量增加比例。多次口服奈玛特韦混悬剂/利托那韦片75mg/100mg~500mg/100mg后,奈玛特韦暴露量增加比例小于剂量增加比例,奈玛特韦在第2天达到稳态。第5天与第10天的暴露相当,蓄积约为第1天的2倍。
吸收
健康受试者单次空腹口服奈玛特韦片/利托那韦片300mg/100mg后,血浆奈玛特韦Cmax、AUClast、AUCinf的几何均值分别为2210ng/mL、22450h·ng/mL、23010h·ng/mL,T1/2为6h,中位Tmax为3h。血浆利托那韦Cmax、AUClast、AUCinf的几何均值分别为359.3ng/mL、3414h·ng/mL、3599h·ng/mL,T1/2为6h,中位Tmax为4h(见附表2)。
与空腹相比,奈玛特韦混悬剂/利托那韦片250mg/100mg与高脂餐同服后,AUC升高约1.5%,Cmax升高约15%(见附表3)。
分布
健康受试者单次空腹口服奈玛特韦片/利托那韦片300mg/100mg后,奈玛特韦和利托那韦的表观分布容积VZ/F分别为109.4L、234.0L。奈玛特韦和利托那韦的人血浆蛋白结合率分别约为69%、98~99%。
代谢
体外研究表明,奈玛特韦是人MDR1(P-gp)和CYP3A的底物,非BCRP、MATE2K、OAT1、OAT3、OATP1B3和OCT2的底物。奈玛特韦主要由CYP3A4代谢,能可逆性和时间依赖性地抑制CYP3A4和MDR1。在临床相关浓度下,奈玛特韦对其它CYP酶无诱导作用,对CYP2D6、CYP2C9、CYP2C19、CYP2C8或CYP1A2无可逆性抑制作用。
人肝微粒体进行的体外研究表明,利托那韦主要是CYP3A的底物,同时也是CYP2D6的底物,CYP2D6参与了异丙噻唑氧化代谢物(M-2)的形成。利托那韦对CYP3A具有抑制作用,对CYP2D6的抑制作用弱于CYP3A。
利托那韦与奈玛特韦联用时,能够抑制奈玛特韦的代谢。奈玛特韦在血浆中主要以原型存在,排泄物(尿液和粪便)存在少量的水解代谢产物M5(12.1%)和M8(4.2%)。
消除
与利托那韦联用时,奈玛特韦主要以原型经肾脏排泄。健康受试者单次空腹口服奈玛特韦混悬剂/利托那韦片300/100mg后,尿液和粪便中的排泄量分别为剂量的49.6%、35.3%。
使用C放射性同位素标记的利托那韦人体研究显示利托那韦主要经肝胆系统清除。粪便中可回收大约86%的放射性同位素标记物,包括部分未被吸收的利托那韦。
不同年龄、体重、性别
尚未考察年龄、体重、性别对奈玛特韦/利托那韦药代动力学的影响。
儿科人群
尚未在年龄<18岁的受试者中开展临床研究。
种族
多次空腹口服奈玛特韦混悬剂/利托那韦片250mg/100mg后,日本受试者的系统暴露低于西方受试者,给药后第5天的稳态AUCtau降低约28%,Cmax降低约23%,Cmin降低约46%(见附表4)。
肾损伤患者
奈玛特韦的暴露量随着肾功能损伤严重程度的增加而增加。
单次空腹口服奈玛特韦片/利托那韦片100mg/100mg后,与肾功能正常受试者相比,轻度(eGFR ≥60至<90mL/min)、中度(eGFR ≥30至<60mL/min)、重度肾功能损伤(eGFR<30mL/min)受试者的AUCinf增加约24%、87%、204%,Cmax增加约30%、38%、48%(见附表5)。
肝损伤患者
尚未在重度肝损伤受试者中开展临床研究。
单次空腹口服奈玛特韦片/利托那韦片100mg/100mg后,与肝功能正常受试者相比,中度肝功能损伤(Child-Pugh Class B)受试者的血浆奈玛特韦的暴露(AUCinf、Cmax)与健康受试者的暴露相当(见附表6)。
在经实验室确诊SARS-CoV-2感染的非住院成人受试者中进行的II/III期、随机、双盲、安慰剂对照的C4671005研究(EPIC-HR 研究)中,共2224例有高风险进展为重症的COVID-19成人受试者,接受了至少一剂奈玛特韦/利托那韦300mg/100mg, n=1109)或安慰剂(n=1115)给药。研究药物每12小时服用一次,持续5天。按照出现频率列出了以下不良反应:
常见的不良反应
指发生频率在≥1/100到<1/10的不良反应。如腹泻、味觉倒错。
偶见的不良反应
指发生频率在≥1/1000到<1/100的不良反应。如消化不良、呕吐、胃食管反流病、肌痛、头晕、丙氨酸氨基转移酶(ALT)升高、天冬氨酸氨基转移酶(AST)升高。
罕见的不良反应
指发生频率在≥1/10000到<1/1000的不良反应。如食欲减退、头痛、嗅觉异常、焦虑、阿弗他溃疡、结肠炎、口干、粪便松软、胸部不适、呼吸困难、呃逆、口咽疼痛、斑丘疹、皮肤剥脱、血促甲状腺激素(TSH)降低。
对奈玛特韦、利托那韦或任何辅料过敏的患者禁用。
不得与高度依赖CYP3A进行清除且其血浆浓度升高会导致严重和/或危及生命的不良反应的药物联用(见附表7)。
不得与强效CYP3A诱导剂联用,否则会显著降低奈玛特韦/利托那韦血浆浓度,可能导致病毒学应答丧失和潜在耐药性(见附表7)。
鉴于CYP3A诱导剂停用后的延迟效应,即使最近停用了附表7中的药物,也不能立即开始该药治疗。
与其他药物相互作用导致严重不良反应的风险
正在接受经CYP3A代谢药品治疗的患者开始服用该药(一种CYP3A抑制剂),或已接受该药治疗的患者开始服用经CYP3A代谢的药品,均可能升高经CYP3A代谢药品的血浆浓度。使用抑制或诱导CYP3A的药品可能会分别升高或降低该药的浓度。
这些药物相互作用可能导致:
有临床意义的不良反应;随着合并用药的暴露量增加,可能导致严重、危及生命或致命性事件。
随着该药的暴露增加,可能出现有临床意义的不良反应。
该药治疗作用的丧失,可能出现病毒耐药的情况。
禁止与奈玛特韦/利托那韦联用的药品见附表7,与该药可能有显著相互作用的其他药品见附表10至附表12。在该药治疗之前和期间应考虑该药与其他药品发生相互作用的可能性;应在该药治疗期间审查合并用药,并监测患者发生的与合并用药相关的不良反应。
严重肾损伤
没有关于严重肾功能损伤患者(包括ESRD患者)的临床数据。根据药代动力学数据(见附表5),在严重肾功能损伤患者中使用该药可能会导致过度暴露,并产生潜在毒性。因此,该药不应用于严重肾功能损伤(eGFR<30 mL/min,包括血液透析下的 ESRD患者。
严重肝损伤
目前尚无严重肝损伤患者的药代动力学和临床数据。因此,该药不应用于严重肝损伤的患者。
肝脏毒性
接受利托那韦治疗的患者曾发生肝转氨酶升高、有临床表现的肝炎和黄疸。因此,既往有肝脏疾病、肝酶异常或者肝炎病史的患者应慎用该药。
出现1型艾滋病病毒(HIV-1)耐药的风险
HIV-1感染未得到控制或未确诊的患者,如果联用奈玛特韦和利托那韦,可能发生HIV-1对HIV蛋白酶抑制剂产生耐药性的风险。
辅料
奈玛特韦片含乳糖。患有半乳糖不耐受、总乳糖酶缺乏或葡萄糖-半乳糖吸收不良等罕见遗传性疾病的患者应禁用该药。
奈玛特韦片和利托那韦片每片钠含量低于1mmol(23 mg),即基本上“无钠”。
对驾驶和操作机器能力的影响
目前尚无评估该药对驾驶和操作机器能力影响的临床研究。
奈玛特韦/利托那韦是CYP3A的抑制剂,可升高由CYP3A代谢的药物的血浆浓度。与奈玛特韦/利托那韦联用时,经CYP3A广泛代谢并具有较高首过代谢的药品可能受影响最大而使自身暴露大幅增加。因此,奈玛特韦/利托那韦不得与高度依赖 CYP3A 进行清除且其血浆浓度升高可能导致严重和/或危及生命的不良反应的药物联用(见附表7)。
在临床相关浓度下,奈玛特韦在体外对CYP2D6、CYP2C9、CYP2C19、CYP2C8 或 CYP1A2无可逆性抑制作用。体外研究结果显示,奈玛特韦可能是CYP3A4、CYP2B6、CYP2C8和CYP2C9的诱导剂,临床相关性未知。基于体外数据,奈玛特韦抑制BCRP、MATE2K、OAT1、OAT3、OATP1B3和 OCT2的可能性较低。在临床相关浓度下,奈玛特韦可能抑制MDR1、MATE1、OCT1和OATP1B1。
利托那韦对几种细胞色素 P450(CYP)亚型具有高度亲和力,并可能抑制其氧化作用,顺序如下:CYP3A4>CYP2D6。利托那韦对 P-糖蛋白(P-gp)也具有高度亲和力,对该转运蛋白具有抑制作用。利托那韦可能诱导CYP1A2、CYP2C8、CYP2C9和CYP2C19的葡萄糖醛酸化和氧化作用,从而增加通过这些途径代谢的部分药品的生物转化,并可能导致此类药品的全身暴露量降低,从而降低或缩短其疗效。
只有在获益大于风险时,才应考虑联用可能产生潜在有意义的相互作用的其他CYP3A4底物。
奈玛特韦和利托那韦是CYP3A的底物,因此,诱导CYP3A的药品可能降低奈玛特韦和利托那韦的血浆浓度,从而降低该药的疗效。
与CYP3A诱导剂卡马西平合用
多次口服卡马西平片100~300mg与奈玛特韦片/利托那韦片300mg/100mg联用后,与单独给药相比,联合给药的奈玛特韦的 AUCinf和 Cmax分别降低约55%和43%。AUCinf、Cmax校正几何均值比的90%CI分别为44.50%(33.77%~58.65%)、56.82%(47.04%~68.62%)(见附表8)。
与CYP3A抑制剂伊曲康唑合用
多次口服伊曲康唑口服溶液200mg与奈玛特韦片/利托那韦片300mg/100mg联用后,与单独给药相比,奈玛特韦的AUCtau和 Cmax分别增加约39%和19%。奈玛特韦的 AUCinf、Cmax校正几何均值比的90%CI分别为138.82%(129.25%~149.11%)、118.57%(112.50%~124.97%)(见附表9)。
影响利托那韦水平的药物
与含有圣约翰草(贯叶连翘)的中草药制剂合用会降低利托那韦血清水平。这是由于圣约翰草(贯叶连翘)能够诱导药物的代谢酶。因此不得将该药与含有圣约翰草(贯叶连翘)的中草药制剂合用。如果患者正在服用圣约翰草(贯叶连翘),应停止服用,如果可能,还应检查病毒水平。停止服用圣约翰(贯叶连翘)草后利托那韦的水平可能会增加,可能需要调整其使用剂量。停止圣约翰草(贯叶连翘)治疗后,其诱导作用可能还会持续至少两周。
利托那韦的血清水平还可能受到合用药物(如地拉韦定,依非韦仑,苯妥英和利福平)的影响。这些相互作用请参见附表10至附表12药物相互作用的列表。
已有报道称,当利托那韦与丙吡胺、美西律或奈法唑酮合用时,出现过心脏和神经系统事件。不能排除药物相互作用的可能。
除了附表10至附表12的药物相互作用,因为利托那韦蛋白结合率较高,应当考虑药物合用时,由于配伍药物蛋白结合置换,可能会增加治疗和毒性反应。
孕妇及哺乳期妇女用药
有生育潜能的女性
尚无妊娠期间使用该药的数据,因而不了解药物相关不良发育结局的风险;育龄女性在该药治疗期间以及治疗结束后 7 天应避免怀孕。
利托那韦与激素类避孕药联用时可能降低后者的疗效。应建议使用复方激素类避孕药的患者在该药治疗期间以及停用该药后的一个月经周期内使用有效的替代避孕方法或额外的屏障避孕方法。
妊娠
没有关于妊娠女性使用该药的数据。只有母亲的潜在获益大于对胎儿的潜在风险时,才能在妊娠期间使用该药。
在大鼠或兔胚胎-胎仔发育毒性研究中检测的任何剂量水平下,奈玛特韦对胎仔形态或胚胎-胎仔存活率无相关影响。
大量妇女在妊娠期间暴露于利托那韦,这表明与基于人群的出生缺陷监测系统中观察到的发生率相比,出生缺陷发生率没有增加。动物实验数据显示利托那韦具有生殖毒性。
哺乳期
目前尚无哺乳期使用该药的数据。尚不清楚奈玛特韦是否会分泌至人或动物乳汁中,及其对母乳喂养的新生儿/婴儿的影响或对乳汁分泌的影响。已发表的数据中,关于人乳中存在利托那韦的报告有限。尚无关于利托那韦对母乳喂养新生儿/婴儿的影响或药物对泌乳量影响的信息。无法排除对新生儿/婴儿的风险。该药治疗期间以及治疗结束后7天应停止哺乳。
生育力
尚无关于该药或单独使用利托那韦对生育力影响的人体数据。奈玛特韦和利托那韦,单独进行试验,对大鼠生育力均未见影响。
儿童用药
该药在18岁以下患者中的安全性与有效性尚不明确。
老人用药
参考成人用药。目前不建议对老年患者进行剂量调整。在 EPIC-HR研究中接受该药治疗的1109例患者中,140 例(12.62%)为 65 岁及以上。
奈玛特韦/利托那韦过量时应予以对症支持性措施,如监测患者生命体征、观察患者的临床状态。该药过量没有特效解毒剂。
2020年7月,科学家首次合成了7mg的奈玛特韦。
2021年3月23日,奈玛特韦/利托那韦进入Ⅰb期临床试验阶段。
2021年4月6日,辉瑞公司在美国化学学会会议上公开奈玛特韦的结构和临床前抗SARS-CoV-2的数据。
2021年11月5日,辉瑞公司公开奈玛特韦/利托那韦Ⅱ/Ⅲ期临床中期试验的疗效结果。
2021年1月16日,辉瑞公司向美国食品药品管理局(FDA)提交奈玛特韦片/利托那韦片组合包装的紧急使用授权(EUA)申请。
该药在经实验室确诊感染SARS-CoV-2的非住院、有症状的成人受试者中开展了一项II/III 期、随机、双盲、安慰剂对照研究(EPIC-HR研究)。该研究纳入受试者为年龄≥18岁,且至少有以下一种进展为重症的高风险因素:糖尿病、超重(BMI>25kg/m)、慢性肺病、慢性肾病、目前吸烟者、免疫抑制疾病或免疫抑制治疗、心血管疾病、高血压、镰状细胞病、神经发育性疾病、活动性癌症、需要相关医疗性支持、或60岁及以上(不考虑合并疾病)。COVID-19症状发作≤5天的受试者被纳入研究。研究排除了既往有COVID-19感染或COVID-19疫苗接种史的患者。
受试者随机(1:1)接受奈玛特韦300mg/利托那韦100mg或安慰剂,口服给药,每12小时1次,持续5天。主要疗效指标是截至第28天内发生COVID-19相关住院或任何原因死亡的受试者比例。样本量共有2246例。该药组和安慰剂组之间的基线人口统计学和疾病特征分布均衡。
Ⅲ期临床试验结果显示,奈玛特韦/利托那韦能将新冠肺炎患者住院率和死亡风险降低89%。
中国《新型冠状病毒肺炎诊疗方案(试行第九版)》将奈玛特韦/利托那韦作为抗病毒治疗药物写入诊疗方案。
奈玛特韦/利托那韦是奈玛特韦片和利托那韦片的组合包装。其中奈玛特韦片的主要成份为奈玛特韦,利托那韦片的主要成为利托那韦。
化学名称
(1R,2S,5S)-N-((1S)-1-氰基-2-((3S)-2-氧代吡咯烷-3-基]乙基)-3-((2S)-3,3-二甲基-2-(2,2,2-三氟乙酰胺基)丁酰基)-6,6-二甲基-3-氮杂双环[3.1.0]己烷-2-甲酰胺
化学结构式
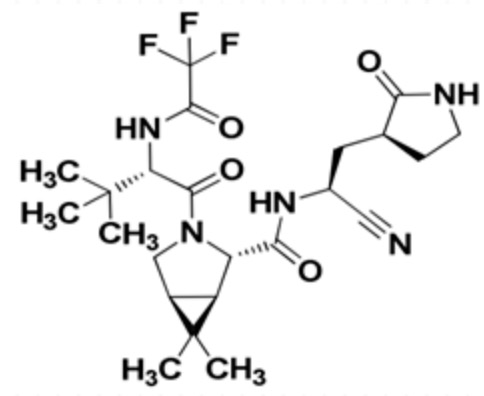
分子式:C23H32F3N5O4
分子量:499.54
性状:粉色椭圆形薄膜衣片,片剂一面凹刻有PFE字样,另一片凹刻有3CL字样,包衣除去后为白色或类白色
化学名称
噻唑-5-基甲基[(1S,2R,4S)-1-苄基-2-羟基-4-[[(2S)-3-甲基-2-[[甲基[[2-(1-甲基乙基)噻唑-4-基]甲基]氨基甲酰基]氨基]丁酰基]氨基]-5-苯基戊基]氨基甲酸酯
化学结构式
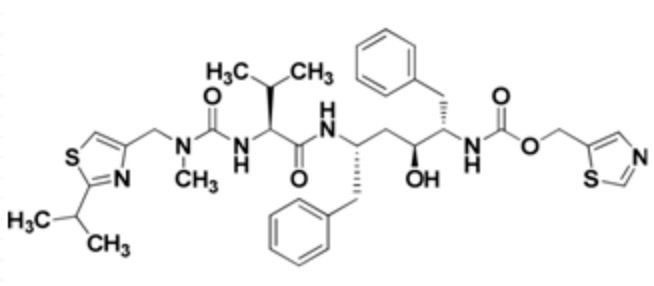
分子式:C37H48N6O5S2
分子量:720.95
性状:白色或类白色薄膜衣片,片剂一面凹刻有H字样,另一片凹刻有R9字样,包衣除去后为白色或类白色
FDA发布EUA,该药的核心成分奈玛特韦(代号PF-07321332)的制备工艺及应用发明专利并非辉瑞制药公司所有,而是美国Prades Biosciences公司所有,且已于2021年4月14日首先申请美国专利和世界知识产权组织进行登记备案。2021年9月21日,US11124497和US11174231已获美国授权,2041年4月14日保护期期满。
基于重大疾病全球流行,FDA允许行使EUA法案,将奈玛特韦片/利托那韦片组合包装的制备工艺专利授权给全球27家制药企业,并将产品提供给全世界95个欠发达、中等发达较贫穷或低收入的国家无偿使用。
2021年12月22日,美国食品药品管理局(FDA)紧急授权奈玛特韦片/利托那韦片组合包装上市,是美国首个治疗COVID-19 的口服药物。
2022年2月11日,国家药品监督管理局(NMPA)按照药品特别审批程序,附条件批准奈玛特韦片/利托那韦片组合包装进口注册。
奈玛特韦/利托那韦与很多药物存在相互作用禁忌,而且在特殊人群中用药尚缺乏安全有效的数据,关于该药是否适用于所有COVID-19患者的临床研究,还需要更多的循证医学证据。
参数 | 奈玛特韦混悬剂/利托那韦片 250/100mg (N=4) | 奈玛特韦混悬剂 250mg (N=4) |
AUCinf(h⋅ng/mL) | 28220(14%) | 3513(38%) |
AUClast(h⋅ng/mL) | 27600(13%) | 3318(35%) |
Cmax(ng/mL) | 2882(25%) | 883.1(37%) |
T1/2(h) | 6.935±1.0794 | 5.626±3.0407 |
Tmax(h) | 2.75(1.50~4.00) | 1.00(0.500~4.00) |
注:表中数据为几何平均值(变异系数%),其中Tmax为中位数(范围),t1/2为算术平均值±标准差。后面表格相同。
参数 | 奈玛特韦片/利托那韦片 300/100mg(N=12) | |
奈玛特韦 | 利托那韦 | |
AUCinf(h⋅ng/mL) | 23010(23%) | 3599(47%) |
AUClast(h⋅ng/mL) | 22450(23%) | 3414(47%) |
Cmax(ng/mL) | 2210(33%) | 359.3(46%) |
T1/2(h) | 6.053±1.7939 | 6.149 ± 2.2413 |
Tmax(h) | 3.00(1.02~6.00) | 3.98(1.48~4.20) |
参数 | 奈玛特韦混悬剂/利托那韦片 250/100mg (空腹) (N=4) | 奈玛特韦混悬剂/利托那韦片 250/100mg (餐后)(N=4) |
AUCinf(h⋅ng/mL) | 28220(14%) | 28640(17%) |
AUClast(h⋅ng/mL) | 27600(13%) | 28020(16%) |
Cmax(ng/mL) | 2882(25%) | 3323(13%) |
T1/2(h) | 6.935±1.0794 | 6.005±1.6502 |
Tmax(h) | 2.75(1.50~4.00) | 4.00(4.00~4.00) |
参数 | 奈玛特韦混悬剂/RTV 250/100mg (西方受试者) (N=4) | 奈玛特韦混悬剂/RTV 250/100mg (日本受试者) (N=4) |
第1天 | ||
AUCtau(h⋅ng/mL) | 18700(43%) | 13130(26%) |
Cmax(ng/mL) | 2435(36%) | 1925(25%) |
Tmax(h) | 1.50(1.00~4.00) | 2.75(1.00~4.02) |
第5天 | ||
AUCtau(h⋅ng/mL) | 35560(26%) | 25480(26%) |
Cmax(ng/mL) | 4774(21%) | 3674(28%) |
Cmin(ng/mL) | 1315(37%) | 707.3(35%) |
Cav(ng/mL) | 2963(26%) | 2124(26%) |
Tmax(h) | 0.75(0.500~1.50) | 1.26(1.00~2.02) |
Rac | 1.901(22%) | 1.937(18%) |
Rac,Cmax | 1.959(16%) | 1.909(26%) |
参数 | 肾功能正常 (N=10) | 轻度肾功能损伤 (N=8) | 中度肾功能损伤 (N=8) | 重度肾功能损伤 (N=8) |
AUCinf(h⋅ng/mL) | 14460(20%) | 17910(30%) | 27110(27%) | 44040(33%) |
AUClast(h⋅ng/mL) | 14270(20%) | 17770(30%) | 26660(21%) | 39420(28%) |
Cmax(ng/mL) | 1600(31%) | 2077(29%) | 2210(17%) | 2369(38%) |
T1/2(h) | 7.725±1.8234 | 6.606±1.5344 | 9.948±3.4171 | 13.37±3.3225 |
Tmax(h) | 2.000 (1.00~4.00) | 2.000 (1.00~3.00) | 2.500 (1.00~6.00) | 3.000 (1.00~6.05) |
参数 | 肝功能正常 (N=8) | 中度肝功能损伤 (N=8) |
AUCinf(h⋅ng/mL) | 15280(36%) | 15070(43%) |
Cmax(ng/mL) | 1890(20%) | 1920(48%) |
T1/2(h) | 7(29) | 5.5(32) |
Tmax(h) | 2(0.5~2) | 1.5(1~2) |
药物类别 | 此类药物中与奈玛特韦/利托那韦配伍禁忌的药物 | 原理 |
合用药物水平升高或降低 | ||
α1肾上腺素能受体拮抗剂 | 阿呋唑嗪 | 阿呋唑嗪的血药浓度增高,可能导致严重的低血压 |
镇痛剂 | 哌替啶,吡罗昔康,丙氧芬 | 去甲哌替啶,吡罗昔康,丙氧芬的血药浓度增高。从而增加严重呼吸抑制、血液系统异常或这类药物所致的其它严重不良反应的发生风险 |
抗心绞痛药 | 雷诺嗪 | 雷诺嗪的血浆浓度升高,可能使发生严重和/或危及生命的不良反应的可能性增加 |
抗癌药 | Neratinib | Neratinib 的血浆浓度升高,可能使发生严重和/或危及生命的不良反应如肝中毒的可能性增加 |
Venetoclax | Venetoclax 的血药浓度增高。在起始剂量及剂量调整阶段肿瘤溶解综合征的风险增加 | |
抗心律失常药 | 胺碘酮、苄普地尔、决奈达隆、恩卡尼、氟卡尼、普罗帕酮、奎尼丁 | 胺碘酮,苄普地尔,决奈达隆,恩卡尼,氟卡尼,普罗帕酮,奎尼丁的血药浓度增高。从而增加心律失常或这类药物所致的其它严重不良反应的发生风险 |
抗生素 | 夫西地酸 | 夫西地酸和利托那韦的血药浓度增高 |
抗真菌药 | 伏立康唑 | 利托那韦(400mg,一日两次和更多次)和伏立康唑禁止合用,因为会降低伏立康唑血药浓度,并可能导致失效 |
抗组胺药 | 阿斯咪唑、特非那定 | 阿斯咪唑和特非那定的血药浓度增高。从而增加了这些药物所致严重心律失常的发生风险 |
抗痛风药 | 秋水仙碱 | 对于有肝损伤、肾损伤患者具有严重不良反应或危及生命的潜在风险 |
抗分枝杆菌药 | 利福布汀 | 利托那韦作为抗反转录病毒药(600mg,一日两次)和利福布汀合用会增加利福布汀的血清浓度和不良反应(包括葡萄膜炎)的发生风险 |
抗精神病药 | 鲁拉西酮 | 鲁拉西酮的血浆浓度升高,可能使发生严重和/或危及生命的不良反应的可能性增加 |
氯氮平、匹莫齐特 | 氯氮平和匹莫齐特的血药浓度增高。从而增加了严重血液学异常或这类药物所致的其它严重不良反应的发生风险 | |
喹硫平 | 喹硫平血药浓度增高,从而导致昏迷。禁止与喹硫平联合用药 | |
麦角衍生物 | 二氢麦角胺、麦角新碱、麦角胺、甲基麦角新碱 | 麦角衍生物血药浓度的增高会导致急性麦角碱毒性,包括血管痉挛和缺血 |
胃肠动力药 | 西沙必利 | 西沙必利的血药浓度增高。将增加该药所致严重心律失常的发生风险 |
血脂调节剂 HMG-CoA还原酶抑制剂 微粒体甘油三酯转运蛋白(MTTP)抑制剂 | 洛伐他汀、辛伐他汀 Lomitapide | 洛伐他汀和辛伐他汀的血药浓度升高;因此增加了包括横纹肌溶解在内的肌病的发生风险。 Lomitapide 的血药浓度升高 |
PDE5抑制剂 | 阿伐那非 | 阿伐那非的血药浓度升高 |
西地那非 | 当作为治疗肺动脉高压(PAH)药物时禁用。西地那非的血药浓度增高。会增加潜在的西地那非相关不良事件(包括低血压和晕厥)的发生风险。在勃起功能障碍患者中与西地那非合用参见【注意事项】和【药物相互作用】 | |
伐地那非 | 伐地那非的血药浓度升高 | |
镇静催眠药 | 氯拉卓酸,地西泮,舒乐安定,氟西泮,口服咪达唑仑和三唑仑 | 氯拉卓酸,地西泮,舒乐安定,氟西泮,口服咪达唑仑和三唑仑的血药浓度增高,从而增加了这些药物所致过度镇静和呼吸抑制的风险 |
奈玛特韦/利托那韦水平降低 | ||
中草药制剂 | 圣约翰草(贯叶连翘) | 由于有降低利托那韦的血药浓度和临床疗效的风险,禁止与含有圣约翰草(贯叶连翘)的中草药制剂合用 |
抗惊厥药 | 卡马西平、苯巴比妥、苯妥英 | 与单独给药相比,联合给药有降低奈玛特韦血药浓度的风险 |
抗感染药 | 利福平 | 利福平是强CYP3A4诱导剂,这可能导致奈玛特韦/利托那韦的暴露减少和病毒学反应的潜在丧失 |
参数 | 奈玛特韦片/利托那韦片 300/100mg(N=12) | 卡马西平+奈玛特韦片/利托那韦片 300/100mg(N=10) |
AUCinf(h⋅ng/mL) | 23010(23%) | 10280(58%) |
AUClast(h⋅ng/mL) | 22450(23%) | 10050(58%) |
Cmax(ng/mL) | 2210(33%) | 1300(43%) |
T1/2(h) | 6.053±1.7939 | 3.845±0.99642 |
Tmax(h) | 3.00(1.02~6.00) | 1.50(0.500~4.00) |
参数 | 奈玛特韦混悬剂/利托那韦片 300/100mg(N=11) | 伊曲康唑+奈玛特韦混悬剂/利托那韦片 300/100mg(N=11) |
AUCinf(h⋅ng/mL) | 41480(21%) | 74430(21%) |
AUClast(h⋅ng/mL) | 33350(20%) | 46290(18%) |
Cmax(ng/mL) | 4678(17%) | 5546(15%) |
T1/2(h) | 8.255±1.9465 | 7.793±0.89019 |
Tmax(h) | 1.020(0.500~2.08) | 1.700(0.500~4.00) |
合用药物 | 合用药物剂量(mg) | 该药剂量(mg) | 评价的药物 | AUC | Cmin |
安泼那韦 | 600 q12h | 100 q12h | 安泼那韦 | ↑64% | ↑5倍 |
利托那韦通过抑制CYP3A4而增加安泼那韦的血清水平。临床试验证实了安泼那韦600mg(一日两次)和利托那韦100mg(一日两次)合用时安全有效 | |||||
阿扎那韦 | 300 q24h | 100 q24h | 阿扎那韦 阿扎那韦 | ↑86% ↑2倍 | ↑11倍 ↑3~7倍 |
利托那韦通过抑制CYP3A4而增加阿扎那韦的血清水平。临床试验证实了在接受过治疗的患者中阿扎那韦300mg(一日一次)和利托那韦100mg(一日一次)合用安全有效 | |||||
达芦那韦 | 600 单剂量 | 100 q12h | 达芦那韦 | ↑14倍 | |
利托那韦通过抑制CYP3A4而增加达芦那韦的血清水平。达芦那韦必须与利托那韦合用才能确保其疗效。尚未研究过利托那韦剂量高于100mg(一日两次)时与达芦那韦合用的情况 | |||||
福沙那韦 | 700 q12h | 100 q12h | 安泼那韦 | ↑2.4倍 | ↑11倍 |
利托那韦通过抑制CYP3A4而增加安泼那韦(来自福沙那韦)的血清水平。福沙那韦必须与利托那韦合用才能确保其疗效。临床试验证实了在接受过治疗的患者中福沙那韦700mg(一日两次)和利托那韦100mg(一日两次)合用安全有效。尚未研究过利托那韦剂量高于100mg(一日两次)时与福沙那韦合用的情况 | |||||
茚地那韦 | 800 q12h 400 q12h | 100 q12h 400 q12h | 茚地那韦 利托那韦 茚地那韦 利托那韦 | ↑78% ↑72% ↔ ↔ | ND ND ↑4倍 ↔ |
利托那韦通过抑制CYP3A4而增加茚地那韦的血清水平。关于有效性和安全性方面,这种联合使用的适当剂量尚未确定。当利托那韦剂量超过100mg一日两次时,其介导的药代动力学增强作用疗效甚微。当联合使用利托那韦(100mg,一日两次)与茚地那韦(800mg,一日两次)时应当慎重,因为可能增加肾石症的风险 | |||||
奈非那韦 | 1250 q12h 750 单剂量 | 100 q12h 500 q12h | 奈非那韦 奈非那韦 利托那韦 | ↑20~39% ↑152% ↔ | ND ND ↔ |
利利托那韦通过抑制CYP3A4而增加奈非那韦的血清水平。关于有效性和安全性方面,这种联合使用的适当剂量尚未确定。当利托那韦剂量超过100mg一日两次时其介导的药代动力学增强作用疗效甚微 | |||||
沙奎那韦 | 1000 q12h 400 q12h | 100 q12h 400 q12h | 沙奎那韦 利托那韦 沙奎那韦 利托那韦 | ↑15倍 ↔ ↑17倍 ↔ | ↑5倍 ↔ ND ↔ |
利托那韦通过抑制CYP3A4而增加沙奎地那韦的血清水平。沙奎那韦只应与利托那韦合用。利托那韦100mg(一日两次)与沙奎那韦1000mg(一日两次)合用时,24小时内沙奎那韦的全身暴露量类似于或超过沙奎那韦1200mg一日三次、不与利托那韦合用时的药物暴露量。在一项研究利福平600mg(一日一次)和沙奎那韦1000mg,利托那韦100mg(一日两次)三者联合应用于健康志愿者中的相互作用的临床研究中,用药1-5天后出现了严重的肝细胞毒性,转氨酶升高超过了正常上限的20倍。由于严重肝脏毒性的风险,不得将沙奎那韦/利托那韦与利福平合用 | |||||
替拉那韦 | 500 q12h | 200 q12h | 替拉那韦 利托那韦 | ↑11倍 ↓40% | ↑29倍 ND |
利托那韦通过抑制CYP3A而增加替拉那韦的血清水平。替拉那韦必须与低剂量的利托那韦合用以确保其疗效。当利托那韦与替拉那韦合用时,剂量不能低于200mg(一日两次),否则可能改变合用疗效 | |||||
ND:未确定 1.基于与单独使用阿扎那韦 400mg(一日一次)的交叉研究比较 2.基于与单独使用安泼那韦 1200mg(一日两次)的交叉研究比较 3.基于与单独使用茚地那韦 800mg(一日三次)的交叉研究比较 4.基于与单独使用沙奎那韦 600mg(一日三次)的交叉研究比较 | |||||
合用药物 | 合用药物剂量(mg) | 该药剂量(mg) | 评价的药物 | AUC | Cmin |
去羟肌苷 | 200 q12h | 600 q12h,2h后 | 去羟肌苷 | ↓13% | ↔ |
由于利托那韦推荐与食物同服,而去羟肌苷应当空腹服用,所以二者的给药时间应当间隔2.5小时。不必改变剂量 | |||||
地拉韦定 | 400 q8h | 600 q12h | 地拉韦定 利托那韦 | ↔ ↑50% | ↔ ↑75% |
与历史数据比较,利托那韦并不影响地拉韦定的药代动力学特性。当与地拉韦定合用时,可以考虑降低利托那韦的剂量 | |||||
依非韦伦 | 600 q24h | 500 q12h | 依非韦伦 利托那韦 | ↑21% ↑17% | |
当利托那韦作为抗反转录病毒药物与依非韦仑依非韦仑合用时,不良事件(如头晕,恶心,感觉异常)及实验室检查结果异常(肝酶升高)的发生频率增加 | |||||
马拉韦罗 | 100 q12h | 100 q12h | 马拉韦罗 | ↑161% | ↑28% |
利托那韦通过抑制CYP3A而增加马拉韦罗的血清水平。马拉韦罗可通过与利托那韦合用而增加马拉韦罗暴露量 | |||||
奈韦拉平 | 200 q12h | 600 q12h | 奈韦拉平 利托那韦 | ↔ ↔ | ↔ ↔ |
利托那韦与奈韦拉平合用时,不会导致奈韦拉平或利托那韦的药代动力学出现具有临床相关性的改变 | |||||
雷特格韦 | 400 单剂量 | 100 q12h | 雷特格韦 | ↓16% | ↓1% |
利托那韦与雷特格韦合用时,会导致雷特格韦水平略微降低。不必改变剂量 | |||||
齐多夫定 | 200 q8h | 300 q6h | 齐多夫定 | ↓25% | ND |
利托那韦可能诱导齐多夫定发生葡萄糖醛酸化,导致齐多夫定水平略降低。不必改变剂量 | |||||
ND:未确定 1. 基于平行组对照 | |||||
合用药物 | 合用药物剂量(mg) | 该药剂量(mg) | 对合用药物AUC的影响 | 对合用药物ACmax的影响 |
α1-肾上腺素能受体拮抗剂 | ||||
阿呋唑嗪 | 与利托那韦合用可能增加阿呋唑嗪的血药浓度,因此禁忌合用 | |||
由于利托那韦推荐与食物同服,而去羟肌苷应当空腹服用,所以二者的给药时间应当间隔2.5小时。不必改变剂量 | ||||
安非他明衍生物 | ||||
安非他明 | 利托那韦作为抗反转录病毒药物使用时,可能抑制CYP2D6,因此预期会增加安非他明及其衍生物的血药浓度。当这类药物与以抗反转录药物剂量给药的利托那韦合用时,应密切监测治疗效应和不良反应 | |||
镇痛药 | ||||
丁丙诺啡 | 16 q24h | 100 q12h | ↑57% | ↑77% |
去甲基丁丙诺菲 | ↑33% | ↑108% | ||
葡糖苷酸代谢产物 | ↔ | ↔ | ||
在阿片类制剂耐受患者中,丁丙诺啡及其活性代谢产物在血浆中浓度的升高不会引起具有临床显著意义的药效学改变。因此当两药合用时不需要调整丁丙诺啡或利托那韦的剂量。当利托那韦与另一蛋白酶抑制剂和丁丙诺啡合用时,具体给药信息请参见所合用蛋白酶抑制剂的产品说明书 | ||||
哌替啶,吡罗昔康,丙氧芬 | 利托那韦合用可能会增加哌替啶,吡罗昔康和丙氧芬的血药浓度,因此禁忌合用 | |||
芬太尼 | 利托那韦作为药代动力学增强剂或抗反转录病毒药物使用时会抑制CYP3A4,从而预期会增加芬太尼的血药浓度。芬太尼与利托那韦合用时,应密切监测疗效和不良反应(包括呼吸抑制) | |||
美沙酮 | 5 单剂量 | 500 q12h | ↓36% | ↓38% |
由于利托那韦能够诱导葡萄糖醛酸化,所以利托那韦作为抗反转录病毒药物或药代动力学增强剂与美沙酮合用时可能需要增加美沙酮的剂量。应当根据患者对美沙酮疗效的临床反应考虑调整剂量 | ||||
吗啡 | 当利托那韦作为抗反转录病毒药物或药代动力学增强剂使用时,可能因为诱导葡萄糖醛酸化,而降低吗啡的水平 | |||
抗心绞痛药 | ||||
雷诺嗪 | 由于利托那韦对CYP3A的抑制作用,预计雷诺嗪的浓度会升高。因此禁忌与雷诺嗪合用 | |||
抗心律失常药 | ||||
胺碘酮,苄普地尔,恩卡尼,氟卡尼,普罗帕酮,奎尼丁 | 利托那韦合用可能导致胺碘酮,苄普地尔,恩卡尼,氟卡尼,普罗帕酮,奎尼丁的血药浓度增加,所以禁忌合用 | |||
地高辛 | 0.5 单剂量静脉 | 300 q12h,3日 | ↑86% | ND |
0.4 单剂量口服 | 200 q12h,13日 | ↑22% | ↔ | |
这种相互作用可能是利托那韦作为抗反转录病毒药物或药代动力学增强剂对 P-糖蛋白介导的地高辛外排作用进行调节的结果。在接受利托那韦治疗的患者中,观察到随着诱导现象的出现,地高辛水平的增加随时间的推移逐渐减弱 | ||||
抗哮喘药 | ||||
茶碱 | 3mg/kg q8h | 500 q12h | ↓43% | ↓32% |
由于利托那韦诱导CYP1A2,合用时可能需要增加茶碱的剂量 | ||||
抗癌药和激酶抑制剂 | ||||
阿法替尼 | 20 单次给药 | 200 q12h/1h前 | ↑48% | ↑39% |
40 单次给药 | 200 q12h/合并给药 | ↑19% | ↑4% | |
40 单次给药 | q12h/6h后 | ↑11% | ↑5% | |
由于乳腺癌耐药蛋白(BCRP)和利托那韦对P-gp的急性抑制作用,可能会导致血清浓度增加。AUC和Cmax增加的程度取决于利托那韦给药的时间。该药与阿法替尼联合用药时应谨慎。应监测与阿法替尼相关的不良反应 | ||||
Abemaciclib | 由于利托那韦对CYP3A4的抑制作用,血清浓度可能增加。应当避免 Abemaciclib 与利托那韦合并用药。如果联合用药被认为不可避免,有关剂量调整建议请参考 Abemaciclib 药品说明书。应监测与Abemaciclib 相关的不良反应 | |||
阿帕他胺 | 阿帕他胺是一种中效至强效CYP3A4诱导剂,这可能导致利托那韦的暴露量降低以及病毒学应答的潜在丧失。此外,与利托那韦合用血清浓度可能增加,可能导致严重不良事件的发生,包括癫痫发作。不建议利托那韦与阿帕他胺合用 | |||
色瑞替尼 | 由于利托那韦对CYP3A和 P-gp的抑制作用,血清浓度可能增加。该药与色瑞替尼联合用药时应谨慎。应监测与色瑞替尼相关的不良反应 | |||
达沙替尼,尼洛替尼,长春新碱,长春碱 | 与利托那韦合用血清浓度可能有所增加,可能导致不良反应的发生率增加 | |||
Encorafenib | 与利托那韦合用血清浓度可能增加,可能会增加发生毒性的风险,包括发生严重不良事件如QT间期延长的风险。应当避免Encorafenib与利托那韦合并用药。如果认为益处超过风险且必须使用利托那韦,则应密切监测在患者中的安全性 | |||
Fostamatinib | Fostamatinib与利托那韦合用可能使Fostamatinib代谢物R406的暴露量增加,导致剂量相关的不良事件,如肝脏毒性、中性粒细胞减少、高血压或腹泻 | |||
伊布替尼 | 由于利托那韦对CYP3A起抑制作用,伊布替尼的血清浓度可能会增加。从而增加包括肿瘤溶解综合征在内的毒性风险。故该药应避免联合使用伊布替尼。如果认为必须使用该药且该联合用药益处超过风险,则将伊布替尼剂量减少至140mg并密切监测患者的毒性 | |||
Neratinib | 由于利托那韦对CYP3A4的抑制作用,血清浓度可能增加。Neratinib与利托那韦禁忌合用,因为可能会增加发生严重和/或危及生命的潜在不良反应如肝中毒的风险 | |||
Venetoclax | 由于利托那韦对CYP3A的抑制作用,血清浓度可能增加,导致在起始剂量及剂量递增阶段肿瘤溶解征的风险增加。对于已完成对Venetoclax的剂量调整处于服用稳定剂量的患者,在使用CYP3A 强抑制剂时Venetoclax的剂量至少减去75% | |||
抗凝药 | ||||
利伐沙班 | 10 单剂量 | 600 q12h | ↑153% | ↑55% |
CYP3A和P-gp的抑制作用会导致利伐沙班的血浆浓度增加并对其产生药效学影响,增加出血的风险。因此不建议正在使用利伐沙班的患者使用利托那韦 | ||||
沃拉帕沙 | 由于利托那韦对CYP3A的抑制作用,血清浓度可能增加。不推荐该药与沃拉帕沙合并用药 | |||
华法林 S-华法林 R-华法林 | 5 单剂量 | 400 q12h | ||
↑9% | ↓9% | |||
↑33% | ↔ | |||
尽管利托那韦对CYP1A2和CYP2C9的诱导作用导致R-华法林水平降低,但联合使用利托那韦对S-华法林的药代动力学几乎没有影响。R-华法林水平降低可能导致抗凝作用减弱,因此建议当利托那韦作为抗反转录病毒药物或药代动力学增强剂与华法林合用时建议密切监测抗凝参数 | ||||
抗惊厥药 | ||||
卡马西平,苯巴比妥,苯妥英 | 卡马西平,苯巴比妥,苯妥英是强效CYP3A4诱导剂,这可能导致奈玛特韦和利托那韦的暴露量降低,并可能导致病毒学反应的潜在丧失,故禁忌合用 | |||
双丙戊酸钠,拉莫三嗪,苯妥英 | 利托那韦作为药代动力学增强剂或抗反转录病毒药物使用时能够诱导CYP2C9介导的氧化作用和葡萄糖醛酸化,因此可能降低抗惊厥药的血浆浓度。当这些药物与利托那韦联合使用时建议密切监测这些药物的血药浓度和疗效。苯妥英可能降低利托那韦的血清水平 | |||
抗抑郁药 | ||||
阿米替林,氟西汀,丙咪嗪,去甲替林,帕罗西汀,舍曲林 | 利托那韦作为抗反转录病毒药物使用时可能会抑制CYP2D6,从而增加阿米替林,氟西汀,丙咪嗪,去甲替林,帕罗西汀或舍曲林的浓度。当这些药物与作为抗反转录病毒药物的利托那韦联合使用时建议密切监测疗效和不良反应 | |||
地昔帕明 | 100 单剂量口服 | 500 q12h | ↑145% | ↑22% |
2-羟基代谢产物的AUC和Cmax分别降低15%和67%。当与作为抗反转录病毒药物的利托那韦合用时,建议降低地昔帕明的剂量 | ||||
曲唑酮 | 50 单剂量 | 200 q12h | ↑2.4倍 | ↑34% |
当利托那韦作为抗反转录病毒药物或药代动力学增强剂与曲唑酮合用时会增加曲唑酮相关不良事件的发生率。如果合用曲唑酮和利托那韦应当慎重,以最低剂量的曲唑酮开始使用,并监测临床反应和耐受性 | ||||
抗痛风药 | ||||
秋水仙碱 | 与利托那韦合用会增加秋水仙碱的浓度。危及生命和致命的药物相互作用在接受秋水仙碱和利托那韦(CYP3A4和P-gp抑制)治疗的患者和肾和/或肝功能不全的患者中已有报道 | |||
抗组胺药 | ||||
阿司咪唑,特非那定 | 与利托那韦作合用时阿司咪唑和特非那定的血药浓度可能增加,因此禁忌合用 | |||
非索非那定 | 利托那韦作为抗反转录病毒药物或药代动力学增强剂使用时可能影响P-糖蛋白介导的非索非那定外排,从而增加非索非那定的血药浓度。所增加的非索非那定水平可能因为诱导作用的出现随时间推移而减弱 | |||
氯雷他定 | 利托那韦作为药代动力学增强剂或抗反转录病毒药物使用时会抑制CYP3A,从而增加氯雷他定的血浆浓度。联合使用氯雷他定和利托那韦时建议密切监测疗效和不良反应 | |||
抗感染药 | ||||
夫西地酸 | 夫西地酸与利托那韦合用时二者的血药浓度均有可能增加,故禁忌合用 | |||
利福布汀 | 150 一日 | 500 q12h | ↑4倍 | ↑2.5倍 |
25-O-去乙酰化利福布汀代谢产物 | ↑38倍 | ↑16倍 | ||
由于利福布汀的AUC会大大增加,因此禁止以利托那韦作为抗反转录病毒药物与利福布汀合用。当利托那韦作为药代动力学增强剂与利福布汀合用时,利福布汀的剂量可能需要减量至150mg(一周三次)以便与指定蛋白酶抑制剂合用 | ||||
利福平 | 利福平是强CYP3A4诱导剂,这可能导致奈玛特韦/利托那韦的暴露减少和病毒学反应的潜在丧失,故禁忌合用 | |||
伏立康唑 | 200 q12h | 400 q12h | ↓82% | ↓66% |
200 q12h | 100 q12h | ↓39% | ↓24% | |
禁止将利托那韦作为抗反转录病毒药物与伏立康唑联合使用,因为这样做会降低伏立康唑的血药浓度。应当避免将利托那韦作为药代动力学增强剂与伏立康唑联合使用,除非对患者的效益/风险评估支持伏立康唑的使用 | ||||
阿托伐醌 | 利托那韦作为药代动力学增强剂或抗反转录病毒药物使用时能够诱导葡萄糖醛酸化,并因此降低血浆中阿托伐醌的浓度。当联合使用阿托伐醌与利托那韦时建议密切监测血清浓度或疗效 | |||
贝达喹啉 | 未与利托那韦单用进行相互作用研究。在一项单剂量贝达喹啉和多剂量洛匹那韦/利托那韦的相互作用研究中,贝达喹啉的AUC增加22%。该增加可能是因利托那韦而产生,且在合并用药延长期间,可观察到该影响更显著。因为具有贝达喹啉相关性不良事件的风险,故应当避免合并用药。如果受益超过风险,则应当在谨慎的情况下进行贝达喹啉与利托那韦的合并用药。建议进行更频繁的心电图监测和转氨酶监测 | |||
克拉霉素 14-羟克拉霉素代谢产物 | 500 q12h | 200 q8h | ↑77% | ↑31% |
↓100% | ↓99% | |||
由于克拉霉素治疗窗宽,所以在肾功能正常的患者中不必减量。当利托那韦作为药代动力学增强剂或抗反转录病毒药物与克拉霉素合用时,克拉霉素的剂量不应超过1克/天。对于肾功能不全的患者,应该考虑对克拉霉素减量:肌酐清除率为30~60ml/min的患者应当减量50%,肌酐清除率低于30ml/min的患者应当减量 75% | ||||
地依麦迪 | 未与利托那韦单用进行相互作用研究。在地依麦迪100mg(每日2次)和洛匹那韦/利托那韦400/100mg(每日2次)给药为期14天的健康志愿者药物相互作用研究中,地依麦迪代谢物DM-6705的暴露量增加30 %。因具有与DM-6705相关的QTc延长风险,故如果认为有必要合并使用地依麦迪与利托那韦,则建议在地依麦迪整个治疗期间,进行更频繁的ECG监测 | |||
红霉素,伊曲康唑 | 利托那韦作为药代动力学增强剂或抗反转录病毒药物使用时会抑制CYP3A4,因此预期会增加血浆中红霉素和伊曲康唑的浓度。当联合使用利托那韦与红霉素或伊曲康唑时建议密切监测疗效和不良反应 | |||
酮康唑 | 200 一日 | 500 q12h | ↑3.4倍 | ↑55% |
利托那韦会抑制CYP3A介导的酮康唑代谢。由于会增加胃肠道和肝脏不良反应的发生率,当利托那韦作为抗反转录病毒药物或药代动力学增强剂与酮康唑合用时,应该考虑降低酮康唑的剂量 | ||||
磺胺甲基异噁唑/ 甲氧苄氨嘧啶 | 800/160 单剂量 | 500 q12h | ↓20%/↑20% | ↔ |
与利托那韦合用时不必调整磺胺甲基异噁唑/甲氧苄氨嘧啶的剂量 | ||||
抗精神病药/精神安定药 | ||||
氯氮平,匹莫齐特 | 与利托那韦合用可能增加血浆中氯氮平或匹莫齐特的浓度,故禁忌合用 | |||
氟哌啶醇,利培酮,硫利达嗪 | 利托那韦作为抗反转录病毒药物使用时可能抑制CYP2D6,并增加氟哌啶醇,利培酮和硫利达嗪的血药浓度。当利托那韦作为抗反转录病毒药物与这些药物合用时建议密切监测疗效和不良反应 | |||
鲁拉西酮 | 由于利托那韦对CYP3A的抑制作用,预计鲁拉西酮的浓度可能会升高,故禁忌与鲁拉西酮合并用药 | |||
喹硫平 | 利托那韦会抑制CYP3A,因此喹硫平的浓度可能会增加。利托那韦和喹硫平合用可能会增加与喹硫平有关的毒性,故禁忌两者合用 | |||
β2 激动剂(长效) | ||||
沙美特罗 | 利托那韦抑制CYP3A4,因此可能导致血浆中沙美特罗的浓度显著升高,故不建议合用。与利托那韦合用可能增加血浆中氯氮平或匹莫齐特的浓度,故禁忌合用 | |||
钙通道阻滞剂 | ||||
氨氯地平,地尔硫卓,硝苯地平 | 利托那韦作为药代动力学增强剂或抗反转录病毒药使用时能抑制CYP3A4,因此预期会增加血浆中钙通道拮抗剂的浓度,联合使用这些药物与利托那韦时建议密切监测疗效和不良反应 | |||
内皮素拮抗剂 | ||||
波生坦 | 波生坦与利托那韦合用可能提高波生坦稳态最高浓度(Cmax)并增加曲线下面积(AUC) | |||
利奥西呱 | 由于利托那韦对CYP3A和P-gp的抑制作用使血清浓度可能增加。不推荐该药与利奥西呱合并用药 | |||
麦角衍生物 | ||||
双氢麦角胺,麦角新碱,麦角胺,甲基麦角新碱 | 与利托那韦合用可能增加血浆中麦角衍生物的浓度,故禁忌合用 | |||
胃肠动力药 | ||||
西沙比利 | 与利托那韦合用可能增加血浆中西沙比利的浓度,故禁忌合用 | |||
HCV直接抗病毒药 | ||||
格卡瑞韦/哌仑他韦 | 由于利托那韦对P糖蛋白、BCRP和OATP1B的抑制作用,格卡瑞韦/哌仑他韦的血清浓度可能增加。由于格卡瑞韦的暴露量增加会增加谷丙转氨酶(ALT)升高的风险,因此不推荐利托那韦与其合并用药 | |||
HCV蛋白酶抑制剂 | ||||
西美瑞韦 | 200 qd | 100 q12h | ↑7.2倍 | ↑4.7倍 |
由于该药对CYP3A4的抑制作用使西美瑞韦血清浓度增加。不建议该药与西美瑞韦合并用药 | ||||
HMG-CoA 还原酶抑制剂 | ||||
阿托伐他汀,氟伐他汀,洛伐他汀,普伐他汀,瑞舒伐他汀,辛伐他汀 | 高度依赖CYP3A代谢的HMG-CoA还原酶抑制剂(例如洛伐他汀和辛伐他汀)在与作为抗反转录病毒药物或药代动力学增强剂的利托那韦联合使用时其血药浓度可能显著增加。由于洛伐他汀和辛伐他汀血药浓度的增加可能导致患者易患肌病(包括横纹肌溶解症),因此这些药物禁忌与利托那韦合用。 阿托伐他汀对CYP3A代谢的依赖程度较低。尽管瑞舒伐他汀的清除不依赖CYP3A,但有报道称瑞舒伐他汀与利托那韦合用时其暴露量有所增加。该反应机制尚不清楚,但可能是转运蛋白受抑制的缘故。当利托那韦作为药代动力学增强剂或是抗反转录病毒药物使用时,阿托伐他汀和瑞舒伐他汀应当采用最低给药剂量。 普伐他汀和氟伐他汀的代谢不依赖CYP3A,并且预期不会与利托那韦相互作用。如果需要采用HMG-CoA 还原酶抑制剂治疗,建议选用普伐他汀或氟伐他汀 | |||
激素类避孕药 | ||||
乙炔雌二醇 | 50μg 单剂量 | 500 q12h | ↓40% | ↓32% |
利托那韦作为抗反转录病毒药物或药代动力学增强剂与乙炔雌二醇合用时会降低乙炔雌二醇的血药浓度,因此合用时应考虑使用避孕工具或非激素类避孕方法。利托那韦可能改变子宫出血情况并降低含乙炔雌二醇的避孕药的有效性 | ||||
免疫抑制剂 | ||||
环孢素,他克莫司,依维莫司 | 利托那韦作为抗反转录病毒药物或药代动力学增强剂使用时会抑制CYP3A4,从而预期会增加环孢素、他克莫司、依维莫司的血药浓度。联合使用这些药物与利托那韦时建议密切监测疗效和不良反应 | |||
血脂调节剂 | ||||
Lomitapide | CYP3A4抑制剂会增加Lomitapide的暴露量,强效抑制剂会导致暴露量增加大约27倍。由于利托那韦能够抑制CYP3A,所以预期会导致Lomitapide的血药浓度增加。禁止合并使用利托那韦和Lomitapide | |||
磷酸二酯酶抑制剂(PDE5) | ||||
阿伐那韦 | 50 单剂量 | 600 q12h | ↑13倍 | ↑2.4倍 |
禁止阿伐那非与利托那韦合用 | ||||
西地那非 | 100 单剂量 | 500 q12h | ↑11倍 | ↑4倍 |
利托那韦作为抗反转录病毒药物或药代动力学增强剂与治疗勃起功能障碍的西地那非联合使用时应该慎重。任何情况下,西地那非在48小时内服用的剂量不得超过25mg。在肺动脉高压患者中禁止联合使用西地那非与利托那韦 | ||||
他达拉非 | 20 单剂量 | 200 q12h | ↑124% | ↔ |
利托那韦作为抗反转录病毒药物或药代动力学增强剂与他达拉非合用应当慎重。应当降低他达拉非的剂量,每72小时内不得超过10mg,同时加强对不良反应的监测 | ||||
伐地那非 | 5 单剂量 | 600 q12h | ↑49倍 | ↑13倍 |
禁止联合使用伐地那非与利托那韦 | ||||
镇静/安眠药 | ||||
氯拉卓酸,地西泮,艾司唑仑,氟西泮,口服或注射用咪达唑仑 | 利托那韦在联合使用时可能会增加血浆中氯拉卓酸,地西泮,艾司唑仑和氟西泮的浓度,故禁忌合用。 咪达唑仑主要通过CYP3A4代谢,与利托那韦合用时可能大大增加这种苯二氮卓类药物的浓度。尚未进行利托那韦与与苯二氮卓类药物合用时药物相互作用的研究。依据其它CYP3A4抑制剂的数据,口服时咪达唑仑在血浆中的浓度显著增高。因此,利托那韦不应与口服咪达唑仑合用,而且利托那韦与非口服咪达唑仑合用时也应当慎重。 关于非口服咪达唑仑与其它蛋白酶抑制剂合用的数据表明,合用时咪达唑仑的血浆水平可能增加3-4 倍。如果需要合用利托那韦与非口服咪达唑仑,应该在重症监护室(ICU)或相似环境中进行,以确保能够进行密切的临床检测并在发生呼吸抑制和/或镇静作用延长时能够采取适当的急救措施。应当考虑调整咪达唑仑的药物剂量,尤其是咪达唑仑的给药次数超过一次时 | |||
三唑仑 | 0.125 单剂量 | 200,4次 | ↑>20倍 | ↑87% |
与利托那韦合用会增加血浆中三唑仑的浓度,故禁忌合用 | ||||
哌替啶 | 50 单剂量口服 | 500 q12h | ↓62% | ↓59% |
去甲哌替啶代谢物 | ↑47% | ↓87% | ||
禁止哌替啶与利托那韦合用,因为合用会增加代谢产物去甲哌替啶的浓度,后者同时具有镇痛和兴奋中枢神经的作用。去甲哌替啶浓度升高可能增加对中枢神经影响(如癫痫发作)的风险 | ||||
阿普唑仑 | 1 单剂量 | 200 q12h,2日 | ↑2.5倍 | ↔ |
500 q12h,10日 | ↓12% | ↓16% | ||
使用利托那韦之后会抑制阿普唑仑的代谢。服用利托那韦10日后,未观察到利托那韦的抑制作用。在阿普唑仑代谢被诱导之前,利托那韦作为抗反转录病毒药物或药代动力学增强剂与阿普唑仑合用的最初数天内应该慎重 | ||||
丁螺环酮 | 利托那韦作为抗反转录病毒药物或药代动力学增强剂会抑制CYP3A,因此预期会增加血浆中丁螺环酮的浓度。当丁螺环酮与利托那韦合用时建议密切监测疗效和不良反应 | |||
催眠药 | ||||
唑吡坦 | 5 | 200,4次 | ↑28% | ↑22% |
在密切监测过度镇静作用的条件下,唑吡坦可与利托那韦合用 | ||||
戒烟药 | ||||
安非他酮 | 150 | 100 q12h | ↓22% | ↓21% |
150 | 600 q12h | ↓66% | ↓62% | |
安非他酮主要通过CYP2B6代谢。安非他酮和多次给药的利托那韦合用时预期可能降低安非他酮的水平。这些作用被认为代表了对安非他酮代谢的诱导作用。然而,利托那韦在体外研究中已经被证实能够抑制CYP2B6,因此不得超过安非他酮的推荐剂量。相对于利托那韦长期用药,短期低剂量利托那韦(200mg,一日两次,服用两日)与安非他酮无显著相互作用,表明利托那韦联合用药数天之后才会出现安非他酮浓度的降低 | ||||
类固醇类药物 | ||||
吸入用、注射用或鼻内给药制剂丙酸氟替卡松,布地奈德,曲安奈德 | 20μg qd | 100 q12h | ↑~350倍 | ↑~25倍 |
已有报道,在接受利托那韦和吸入或鼻喷丙酸氟替卡松的患者中出现过全身皮质类固醇反应,包括库欣综合征和肾上腺抑制(上述研究中皮质醇血浆水平降低86%);在依赖CYP3A代谢的其它皮质类固醇(如布地奈德和曲安奈德)中也观察到类似反应。因此不建议利托那韦作为药代动力学增强剂或抗反转录病毒药物与这些糖皮质激素联合使用,除非治疗的可能益处超过了皮质类固醇全身反应的风险。合用时应当考虑降低糖皮质激素剂量并密切监测全身或局部反应,或者换用不是CYP3A4底物的其它糖皮质激素(如倍氯米松)。此外,糖皮质激素撤药时需逐步降低剂量到最后停用,所需时间可能会较长 | ||||
地塞米松 | 利托那韦作为药代动力学增强剂或抗反转录病毒药物会抑制CYP3A,因此能够增加血浆中地塞米松的浓度。联合使用地塞米松与利托那韦时建议密切监测疗效和不良反应 | |||
泼尼松龙 | 20 | 200 q12h | ↑28% | ↑9% |
泼尼松龙与利托那韦合用时,建议密切监测疗效和不良反应。与利托那韦合用4和14天后,泼尼松龙代谢物的AUC分别增加37%和28% | ||||
甲状腺激素替代疗法 | ||||
左旋甲状腺素 | 据上市后案例表明,含有利托那韦的产品和左甲状腺素之间存在潜在的相互作用。使用左旋甲状腺素治疗的患者应监测甲状腺激素(TSH),至少是在开始和/或结束洛匹那韦/利托那韦使用后的第一个月 | |||
ND:未确定 1:基于平行组对照 2:磺胺甲基异噁唑与甲氧苄氨嘧啶合用 | ||||
AUC:全称为area under curve,即血药浓度-时间曲线下面积,表示一段时间内药物在血浆中的相对积累量。
AUCinf:是指时间从0时至无穷大时血药浓度-时间曲线下面积。
AUClast:是指时间从0 时到指明时间区域内最后一次可测浓度时血药浓度-时间曲线下面积。
AUCtau:是指给药间隔内的AUC。
Cmax:全称为maximum concentration,即达峰浓度,是指血管外给药后药物在体内所能达到的最高血药浓度。
Cmin:全称为minimum concentration,即最小有效浓度,即血管外给药后药物在体内的最小有效浓度。
Cav:是指平均稳态血药浓度。
T1/2:全称为Elimination half life,即半衰期,是指药物在体内的量或血药浓度下降一半所需的时间。
Tmax:全称为time to reach maximum concentration,即达峰时间,即药物在体内达到最高血药浓度所需的时间。
Rac:全称为accumulation index,即蓄积指数或累积指数,是一个比值。一般而言,在连续给药条件下,6~7个半衰期后,药物谷浓度(每次给药前浓度)可达稳态。此时血药浓度将在稳态谷浓度基础上增加,不仅药物在体内的积累量(AUC)较首次给药明显增加,同时药物的峰浓度(Cmax)也将高于首次给药,这种现场称为药物的蓄积或积累。
Rac(Cmax):是指Cmax药物蓄积比,用Cmax末剂与Cmax首剂计算。
表观分布容积:是体内药量与血药浓度间的一个比例常数,用来描述药物在体内分布的程度。
VZ/F:指基于末端消除相计算的分布容积,表示血管外给药经生物利用度校正的表观分布容积。
[b]药物在体内的累积
新亚洲娱乐(英文名:ASIA ENTERTAINMENT GROUP LIMITED,全称:新亚洲娱乐联盟集团有限公司)是一家以从事戏剧制作人及杂项戏剧服务为主的企业,成立于1999年,位于香港特别行政区。旗下分公司包括虎威艺能创作有限公司(TGS HK)、稻草人娱乐创作社(Scarecrow Entertainment)、虎威王朝音乐创作股份有限公司(TGS Music)、虎威活力娱乐传播有限公司(TGS Taiwan)、AK Entertainment(Korea)以及AEG Korea等。
印度孟买SENSEX30指数(又称孟买敏感指数)为印度最被广泛使用的指数,为投资印度的重要参考指标,是由孟买证券交易所发行。由于各类媒体提到的“印度股市”,实际上都是孟买股票交易所,因此,该交易所的SENSEX-30指数几乎成了印度股市的代名词。