发现历史
1787年,业余矿物学家、瑞典陆军中尉阿伦尼乌斯(Carl Axel Arrhenius)在瑞典首都斯德哥尔摩附近的伊特比(Ytterby)村发现一种黑石,1794年,芬兰化学家加多林(J.Godolin)从此矿物中分离出一种新的土性化合物,其含量达 38%,并根据矿石原产地是伊特比而将这种土性化合物称为“钇土”(yttria)。为了纪念加多林的贡献,该矿石被称为硅铍钇矿。随后,安德斯·古斯塔夫·埃克贝格(Anders Gustav Ekeberg)在此矿物中发现了一种新元素,将其命名为 Yteelium,这是人类最早确定的稀土元素。1803 年,德国人克莱普罗斯 (MHKaproth)、瑞典人贝采里乌斯(J.J.Berzelius)和希辛格尔 (WHisinger)在其他矿石中发现了第二种稀土元素,它们将其命名为“铈土”(ceria)。在之后的100余年里,人们发现“钇土”和“铈土”并非单一元素,而是混合氧化物。随着工艺的进步,人们逐渐从“钇土”和“铈土”中分离和鉴定出剩余的14个稀土元素。此外,“钇土”和“铈土”并非是稀有元素的单质,而是它们的氧化物。1945年,最后一个稀有金属钜(Pm)于美国发现,所有稀土元素被确定下来。
分布存在
钇在地壳中的丰度为0.0028,排在所有元素的第30位,在稀土元素中仅次于铈,排在第二位。在自然界中,钇与其余稀土元素紧密结合,共同赋存于相同的矿物中,主要有三种形态。第一种为独立稀土矿物,如氟碳矿、独居石等,主成分为稀土元素;第二种为含有稀土元素的其余矿物如磷灰石、萤石等,第三种矿物中,稀土元素主要以离子状态吸附。世界上已知的稀土矿物约有 150 种之多,而含有稀元素的矿物有 250种以上。不同种类的矿物中各类稀土元素的配分差异较大。元素钇在磷钇矿、褐钇铌矿中含量较高,这些矿物也是提取金属钇的主要原料。
稀土矿物在世界范围内分布差异较大,根据2018年美国地质勘探局 (United States Geological Survey,USGS)的数据,在全球稀土总储量中,中国约占38%,巴西占19%,越南占19%,俄罗斯占 10%,印度占 6%,美国等其他国家占 8%。在产量方面,2017年中国年产量占世界生产总量的80%以上,大部分的钇产品(氧化钇)也主要来自于中国。工业上的主要矿物包括氟碳铈矿、独居石、磷矿、离子型稀土矿等,这几种矿占稀土产量 95%以上。
物质结构
钇是周期表中IIIB族元素,与钪、镧系同属于稀土元素。钇的化学式为Y,原子序数为39,摩尔质量为88.90g/mol,原子体积为33.7cm/mol,原子密度为4.47g/cm,钇原子的核外电子排布为[Kr]4d5s(1s2s2p3s3p3d4s4p4d5s),最外层有2个电子,次外层只有一个电子,活跃电子数为3,在自然界中主要以+3价态存在。钇在自然界中仅存在一种稳定的同位素Y,此外还有30种放射性同位素以及16种同质异能素。与大多数稀土金属类似,钇呈紧密六方晶格或面心立方晶格结构排布。
理化性质
物理性质
金属钇是一种质软、带光泽的银白色金属晶体,无味,粉末状态时呈黑色。成块的钇在空气中会在表面形成保护性氧化层(Y2O3),这种钝化过程使它相对稳定。不过粉末在空气中很不稳定,金属屑可以在 400℃以上的温度在空气中点燃。钇的熔点为1509℃,沸点为2927℃,20℃时密度为4.47,在水和盐酸、硫酸中分解。
化学性质
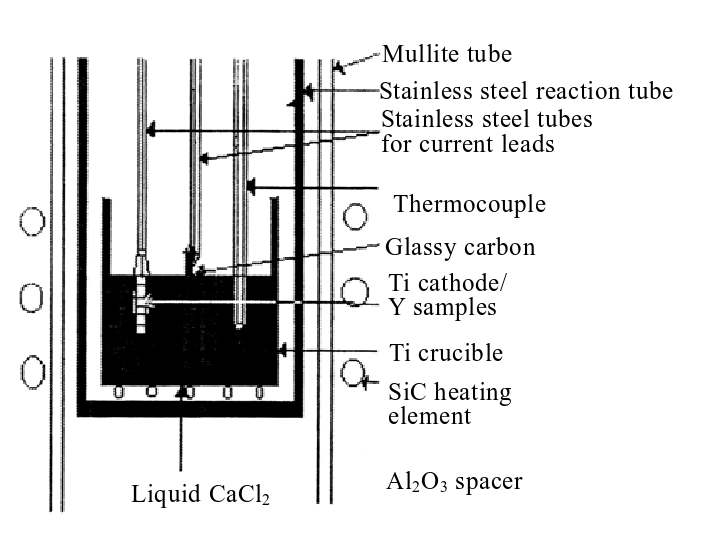
金属热还原法利用的是钇的氟化物或者氯化物与金属还原剂在反应槽内加热发生反应制备单质钇,右图为热还原法使用的反应槽,还原剂一般采用钙、镁和钾,其中,钾、镁用于氯化物的还原,钙主要用于氟化物的还原,后者也被称为钙热还原法,具有速率快,产物回收率高的优点。
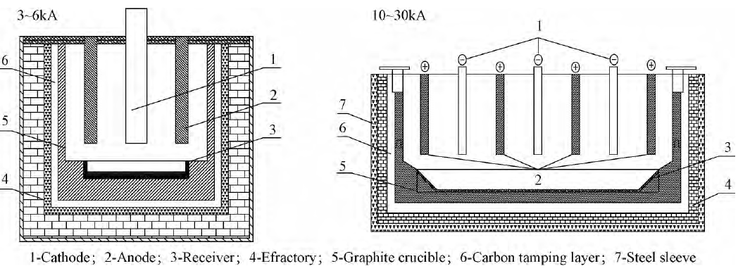
熔盐电解法主要采用的是氯化钇和碱金属氯化物熔盐体系,具有成本低,利用率高等特点。右图显示了两种常用的电解槽,其中阴极一般采用钜或钨材料制成,阳极由石墨烯制成,反应过程涉及的主要方程式如下:
阳极:
阴极:

钇的危险标识图,资料来源于: |
GHS | 危险说明 | 危险等级 |
H228 (75.76%) | 易燃固体 | 危险 易燃固体 |
H250 (49.49%) | 如果暴露在空气中会自燃 | 危险 自燃液体 自然固体 |
H302 (47.47%) | 吞食有害 | 警告 急性毒性 口服 |
H312 (47.47%) | 与皮肤接触有害 | 警告 急性毒性 皮肤 |
H332 (47.47%) | 吸入有害 | 警告 急性毒性 吸入 |
H371 (13.13%) | 可能对器官造成损害 | 警告 特定目标器官毒性,單次接触 |
H413 (19.19%) | 对水生生物造成长期影响 | 对水生环境有害,长期危害 |
锶的GHS分类,资料来源于: |
储存与运输
金属钇应该保存在干燥环境中,或使用惰性气体保护,并存放在通风良好的房间内。存放地点需远离排水管或下水道等地方。在运输过程中要注意保持容器密闭,做好防潮,使用惰性气体保护。
火灾风险与处置
金属钇可被摩擦、热量、火花或火焰点燃。有些可能会迅速燃烧,有耀眼的燃烧效果。粉末、粉尘、刨花、钻孔、车削或切割物可能会爆炸或以爆炸性的暴力燃烧。物质可能以熔融形式运输,温度可能高于其闪点。火灾扑灭后可能重新点燃。
如果金属钇不慎燃烧,在火情较小时,可使用干化学剂、二氧化碳、沙子、土、喷水或普通泡沫。如果火情较大,应使用喷水、雾化或普通泡沫。在安全的前提下,将未损坏的钇储存容器撤离火场,如果火情无法控制,迅速撤离。
健康危害与处置
钇可以通过皮肤、呼吸道、眼睛、饮食等进入人体。如果眼睛不慎与钇接触,立即用大量水清洗,偶尔抬起下眼睑和上眼睑,并迅速就医。如果皮肤与钇接触,立即用肥皂和水清洗受污染的皮肤。如果渗透到衣服中,立即脱掉衣服并用肥皂和水清洗皮肤,并及时就医。如果不慎吸入大量这种化学物质,请立即将暴露的人转移到新鲜空气中,如果呼吸停止,请进行人工呼吸。让受影响的人保持温暖和休息。尽快就医。如果不慎吞咽,需要立即就医。
毒理学资料
大鼠单次气管内给药后出现肺纤维化;在动物研究中,通过腹腔途径有中度毒性;50毫克/千克的剂量会导致肝脏坏死。在鼠体实验中,静脉注射Y20微居里/克,给狗静脉注射Y,剂量为0.1~0.2微居里/公斤,白细胞、红胞及血小板数均出现降低。狗由于放射病在存活26天后死亡,观察到骨骼发育不全。给大鼠剂量为0.6微居里/克时,在60~75%的动物中引起骨肉瘤。