简介
热力学第二定律的发展历程与蒸汽机的发展和推动有关。在1768年瓦特改进蒸汽机之前,热机效率非常低,即使改进后,也不超过5%。随后,人们采取了各种措施来提高热机效率,并取得了一些成果。1824年,法国工程师卡诺(N.L.S. Carnot)在他的论文《论火的动力》中提出了热机效率存在一个极限,即卡诺定理。1850年,德国的克劳修斯(R.J.E. Clausius)也研究了卡诺的工作,发现要证明卡诺定理需要一个新的自然规律,即热力学第二定律。1851年,开尔文也得出了热力学第二定律,其内容否定了第二类永动机的存在。1865年,克劳修斯从分析热力学第二定律的推论开始,研究了卡诺定律,得出了克劳修斯等式。
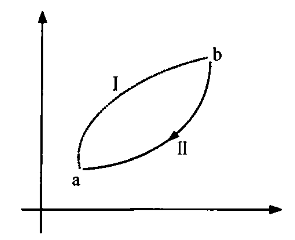
熵增原理给出了热力学第二定律的定量描述,此描述由克劳修斯于1865年提出,他找到了一种数学方法来表示可逆与不可逆循环过程中总熵的变化。熵是系统状态的函数,其变化仅由系统的初始和最终状态决定,与路径无关。
定义
热力学第二定律有多种表达方式。无论何种表达方式,都描述的是自然过程的方向性和不可逆性。
开尔文表述
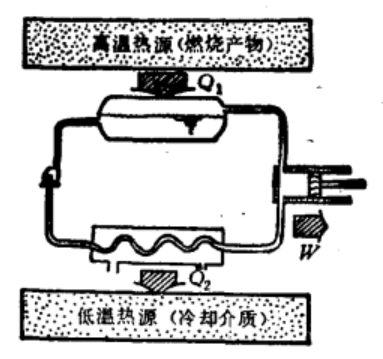
大量实践经验表明,热机在将吸收的热量转化为有用功的同时,无法避免地向低温热源释放一部分热量,因此效率必然小于100%。基于这些实践经验,开尔文于1851年提出了热力学第二定律的第一种表述,即开尔文表述:不可能制成一种循环动作的热机,只从单一热源吸收热量,使其完全变为有用功而不产生其他影响。
从单热源吸取热量并将其全部转化为有用功而不产生其他影响的热机被称为第二类永动机。因此,热力学第二定律的开尔文表述可以简化为:第二类永动机是不可能实现的。
克劳修斯(R.L.E.Clausius)表述
克劳修斯将热力学第二定律表述为:不可能把热量从低温物体传到高温物体而不产生任何其他影响。
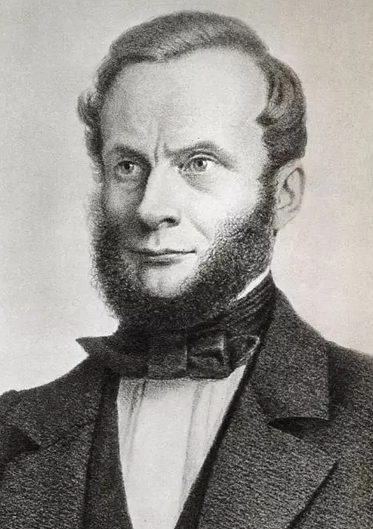
其他表述
热力学第二定律的一种表达方式为:隔离系统中,自发过程是向混乱度增加的方向进行。当熵增加至极大值时,系统达到平衡状态。
其中,隔离系统指的是所研究的系统与相关的环境,因此有:
原理
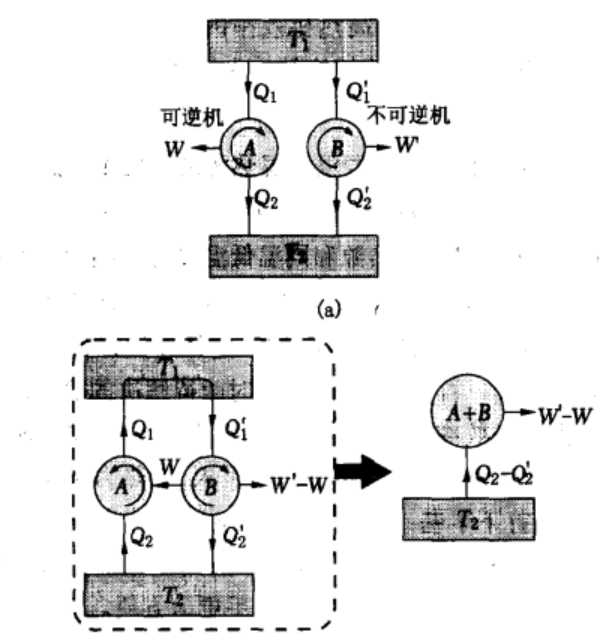
卡诺定理
卡诺定理是热力学中的一个重要定理,描述了热能转化效率的上限。它是由法国工程师尤尔·卡诺(Sadi Carnot)于1824年首次提出的,被认为是热力学的一个基本原理。
卡诺定理的主要内容可以总结为以下几点:
热源与冷源: 卡诺定理考虑了两个温度不同的热源,一个高温热源和一个低温热源,它们之间有一个工作物质(例如气体)在循环过程中工作。
循环过程: 卡诺定理描述的是一个理想的循环过程,称为卡诺循环。卡诺循环包括两个等温过程和两个绝热过程,形成一个闭合循环。
热能转化效率: 卡诺定理指出,在所有可能的热能转化过程中,卡诺循环所对应的热能转化效率是最高的。这意味着,在给定温度下,没有任何热能转化过程能够比卡诺循环的效率更高。
卡诺效率公式: η = 1 - (Tc/Th)
其中,η是卡诺效率,Tc是冷源的温度,Th是热源的温度。
卡诺定理的重要性在于它提供了理论上的热能转化效率的上限,帮助人们理解能源转换和热力学效率的极限。尽管实际系统无法完全达到卡诺效率,但卡诺定理仍然为工程和科学研究提供了重要的参考依据。
热力学温标
热力学温标是基于热力学原理而建立的温度刻度,完全不依赖于特定物质的性质,是一种理论上的理想温标。它由开尔文(Kelvin)在热力学第二定律的基础上提出,并与实际测温物质的性质无关,因此脱离了经验温标的范畴。尽管难以直接实践,热力学温标在国际上被认定为基本温标,因为它具有严密的理论基础和定义。热力学温标与理想气体温标在理论确定的温度范围内具有相等的温度值,因此在一定条件下可以通过理想气体温标来实现。此外,热力学温标的温度值还在物理学方程中发挥重要作用,例如在普朗克黑体辐射定律和聂奎斯脱噪声方程等中。热力学温标分为开尔文温度和摄氏温度。开尔文温度是基本温度单位,用“K”表示,定义为水的三相点热力学温度的1/273.16。热力学摄氏温度则由开尔文温度导出,其单位为℃,1℃的温度间隔与1K相等。总之,热力学温标是基于热力学原理的理论温标,具有重要的理论和实际应用价值。
克劳修斯定律与熵
热力学第二定律对热力学系统中宏观过程的转化方向进行了定性描述,揭示了宏观自然过程的方向性。熵增原理给出了热力学第二定律的定量描述,此描述由克劳修斯于1865年提出,他找到了一种数学方法来表示可逆与不可逆循环过程中总熵的变化。
将
适用条件
热力学第二定律探讨的是大量粒子组成的有限系统的行为,但并不适用于无限的宇宙。在当时的研究中,也留下了关于热力学第二定律是否适用于生命界的问题。
适用于范围有限的粒子
热力学第二定律适用于范围有限的系统,并且通过正确运用该定律,我们得出的结论与实际事实是相一致的。然而,如果我们将该定律的使用范围无限外推到整个宇宙,就会得出克劳修斯的所谓“热寂说”。这种说法认为将无限的宇宙视为一个孤立系统,并将热力学第二定律应用于宇宙,得出宇宙的熵永远增加的结论。这就意味着宇宙会趋向于一个平衡状态,越接近这个平衡状态,宇宙的无序程度就越大,最终导致宇宙进入死寂的永恒状态。这个“热寂说”犯了一个错误,它将有限范围内得到的客观规律无根据地外推到了无限的宇宙。有限的系统和无限大的宇宙是两种性质根本不同的系统。在有限系统内成立的客观规律,在无限大的宇宙中未必能够成立。
适用于大量微观粒子组成的系统
热力学第二定律是通过大量实验事实总结出来的,适用于时间与空间都有限的宏观系统。这些宏观系统由许多微观粒子组成。然而,对于由少数原子或分子组成的系统,例如只有三个分子的系统,热力学第二定律并不适用。热力学第二定律涉及一些物理概念,比如温度和熵。温度是大量微观粒子热运动的集体表现,与这些粒子运动的平均能量有关,具有统计意义。在统计物理中,熵也具有统计意义。然而,在物理学中,统计规律只对大量粒子组成的体系成立,而少数原子或分子组成的系统并不遵循统计规律。因此,热力学第二定律不适用于由少数原子或分子组成的体系。
生命现象的挑战
生命体是属于有限范围内的宏观物体,因此热力学第二定律适用于描述生命体的行为。然而,在耗散结构理论刚创立之前,生命现象对热力学第二定律似乎是一个例外。生命体处于非平衡状态,生命过程是不可逆的。根据热力学第二定律,对于生命体来说,其熵的变化总是大于吸收的热量除以温度的乘积。这意味着生命过程伴随着熵的增加,从而导致生命体的有序度降低或由有序状态转向无序状态。然而,根据达尔文的进化论,生命现象朝着由简单到复杂、由低级到高级、由无序向有序的方向发展。正因为这种矛盾,一些人认为热力学第二定律只适用于无生命的物体,而不适用于生命体。
幸运的是,比利时布鲁塞尔自由大学的伊·普利高津教授创建了耗散结构理论来解决这个问题。耗散结构理论认为,对于一个开放系统,熵的变化可以分为两部分,一部分是由系统本身的不可逆过程引起的熵增加(即熵产生),这部分总是正的;另一部分是系统与外界交换物质和能量引起的熵流,这部分可以是正的也可以是负的。整个系统的熵的变化等于这两部分之和。如果外界的负熵流足够大,能够抵消系统本身的熵产生,那么整个系统的熵变就会小于零。这意味着系统可以逐步从无序向新的有序方向发展,最终形成一个低熵的有序结构,并通过与外界的物质、能量交换来维持这种有序结构。生命体是一种远离平衡态的开放系统,它依靠从外界获取物质和能量来维持自身的有序性。这样,生命体从外界获取物质和能量的效果相当于从外界获得了负的熵流,因而可以抵消体内由于不可逆过程引起的熵增加。普利高津因其对耗散结构理论的重大贡献,获得了1977年诺贝尔化学奖。

研究进展
对多过程体系中热力学耦合现象的认识促使热力学第二定律的研究有了实质性发展。
20世纪30年代,热力学第二定律的研究出现了明显的变化,重点在于对多过程体系中热力学耦合现象的认识。在研究不可逆过程时,我们观察到了反常的扩散(过程1,是非自发过程)和正常的热传导(过程2,是自发过程)可以同时进行的热力学耦合现象,也称为热扩散现象。1931年Onsager提出了倒易关系式,开拓了线性耗散热力学的新领域。
在20世纪50年代,科学家们观察到了在远离平衡条件下出现的化学振荡等宏观有序化现象。这激发了Prigogine提出宏观有序化过程(非自发过程)和耗散过程(自发过程)同时存在的耗散结构。这一理论开创了非线性耗散热力学的新领域。
在20世纪70年代,出现了一种新的金刚石合成工艺,称为激活(非平衡)低压金刚石合成。然而,由于一些错误的热力学传统观念,这个新工艺遇到了很多困难,直到1986年,广大的学者们才公认和接受了这个新工艺的实验事实。在1990年,王季陶与瑞典学者J.-O.Carlsson一起发表了激活低压金刚石合成热力学耦合模型的第一篇文章。这个模型涉及从石墨转变为金刚石的低压过程(非自发过程)和超平衡原子氢缔合成氢分子的过程(自发过程),并按照热力学耦合的规律进行处理。经过王季陶和合作者长达10多年的持续研究,他们得到了一系列激活低压金刚石生长的非平衡相图,并最终开创了一个新的领域——非平衡非耗散热力学。
上述20世纪30年代以来得到的三个热力学新领域共同组成了现代热力学。
应用
热力学定律在各行各业都有应用,以下仅举例部分。
换热器性能研究:评价换热器性能虽然重要,却也很复杂,因为它不仅与性能相关,还与形状和大小有关。这对设计和选择都很关键。利用热力学第二定律的方法,我们可以将传热和阻力这两个因素转化成容易计算的熵增和功率值。通过这种方式,我们可以更深入地分析换热器的工作过程,得出适当的评价标准。基于这个分析,我们可以更好地理解两个评价标准:效率(J)和可用性(U)。这两个标准涵盖了熵增这个物理概念,而且存在最优值,方便实际计算。这种分析方法对于指导换热器的研究、设计和使用都有很大的帮助。

余热资源研究:余热是指在工艺系统或设备中产生的能量,由于难以有效利用而被排出系统外。由于这部分能量很大,在如今强调节能减排的时代,人们越来越重视如何利用这些未被充分利用的能量。目前,虽然人们在研究如何利用余热的新技术和方法方面付出了很多努力,但往往忽略了对余热资源及其利用的热力学分析方法的研究。现有的热力学分析方法主要基于热力学第一定律,而基于热力学第二定律的分析方法相对较少。然而,基于热力学第二定律的方法更科学和合理,特别是对于低品位热能如余热的分析。仅仅根据余热的绝对量来计算节能贡献可能是片面的,因此我们迫切需要科学地计算余热回收利用的实际节能效果。
研究意义
热力学第二定律是热力学中的重要定律,其研究意义包括以下几个方面:
方向性:热力学第二定律揭示了自然过程的方向性,指出自然现象总是趋向于熵的增加或系统的混乱增加。这对于理解自然界中各种过程的进行方向具有重要意义。
不可逆性:该定律说明自然界中的大部分过程都是不可逆的,无法逆转发生。这为我们提供了认识自然界的限制,也解释了为什么有些过程无法回到原来的状态。
热机效率:热力学第二定律对热机的效率提出了限制,即不能将热能全部转化为有用的功,一定会有一部分热能转化为熵增,从而限制了能源利用效率。
能源管理:热力学第二定律对能源管理和节能有指导意义。它告诉我们在能量转化和利用过程中,存在能量的损耗和不可避免的能量转化方向,因此需要在能源利用中寻求更高效率和更可持续的方式。
热平衡与热力学平衡:该定律帮助我们理解系统达到热平衡或热力学平衡的条件,以及不同系统之间的热平衡状态。