简介
该药的不良反应主要为胃肠道轻度不适,偶有恶心、呕吐、消化不良、便秘、胃肠道出血等。与阿司匹林等非甾体抗炎药有交叉过敏反应。该药禁用于对同类药物过敏者,消化性溃疡、孕妇、哺乳妇、2岁以下儿童、冠状动脉搭桥围术期患者也需禁用。慎用于凝血功能障碍,哮喘,心、肝、肾功能不全,胃肠道疾病,老年患者,脱水患者,有贫血史患者。
萘普生有多种剂型,包括片剂、胶囊、颗粒、栓剂、注射液等,属于医保乙类药物。美国食品药品监督管理局(FDA)提示:在孕20周或之后使用包括萘普生在内的非甾体抗炎药(NSAIDs)可导致罕见且严重的胎儿肾脏问题,可能引起宫内羊水不足并出现并发症。
医学用途
适应症
用法用量
成人
儿童
抗风湿:一日10-20mg/kg,分2次口服,单日剂量≤2g。
制剂与规格
萘普生片:0.1g;0.125g;0.25g。
茶普生胶囊:0.1g;0.125g;0.2g;0.25g。
萘普生缓释片:0.25g;0.5g。
蔡普生缓释胶囊:0.25g。
萘普生颗粒:10g∶0.25g。
萘普生栓:0.25g;0.3g;0.4g。
萘普生注射液:2ml:0.1g;2ml:0.2g。
萘普待因片:每片含萘普生150mg,磷酸可待因15mg。
药理机制
萘普生为非甾体类抗炎镇痛药(NSAIDs),疗效与布洛芬基本相同,抗炎和镇痛的机制也是由于抑制前列腺素的合成。
镇痛抗炎:主要通过抑制炎症细胞的花生四烯酸代谢物——环氧酶(cyclo-oxygenase,COX),减少炎症介质——各类前列腺素和血栓素的合成。在炎症部位的前列环素(PGI2)具有的血管扩张作用促使局部组织充血肿胀,前列腺素E又可增强该处受损组织痛觉阙的敏感度,构成炎症部位肿痛炎症症状。当COX被NSAIDs抑制后,各类前列腺素的合成减少,临床肿痛症状得以改善,这与中枢镇痛药单纯镇痛的作用机制不同。
解热:人体体温调节中枢位于下丘脑,调控产热和散热过程,维持动态平衡,使体温维持正常。病理条件下,发热原(外热原)如病原微生物(细菌、真菌、病毒)、非微生物抗原、炎症渗出物、致热性类固醇等,刺激机体血液中的单核细胞和组织中的巨噬细胞产生并释放内生性致热原(简称内热原),如IL-1、TNF、IL-6等。传统观点认为,内热原直接作用于下丘脑,使产热增加,散热减少,从而引起发热。而John Vane在研究中发现,内热原不能直接作用于下丘脑引起发热,而是引起下丘脑PGs的合成和释放,将微量的PGE2直接注入脑室或下丘脑前部,即可引起体温升高。而且在发热同时,脑脊液中PGE样物质增高2.5-4倍。因此,内热原作用于下丘脑视前区引起PGE2合成和释放增加,PGE2作为中枢性致热原作用于体温调节中枢,使调定点上移,引起发热。实验证明,NSAIDs对脑室内注射微量PGE2引起的机体发热无效,而对内热原所致的发热有效,这说明NSAIDs的解热作用部位在下丘脑,通过抑制下丘脑COX,阻断PGE2合成,使体温调节中枢的调定点恢复正常,发挥解热作用。因此,NSAIDs只能降低发热者的体温,不影响正常人的体温。
药代动力学
该药的蛋白结合率高于99%。t1/2一般为13小时。止痛作用开始时间为1小时,持续7小时。抗风湿作用最长可达14天。
风险与禁忌
不良反应
该药的不良反应主要为胃肠道轻度不适。偶有恶心、呕吐、消化不良、便秘、胃肠道出血等,一般不需中断治疗。该药与阿司匹林和吲哚美辛比较,症状缓解的效应相仿,但胃肠道和神经系统的不良反应的发生率和严重程度均较低。
药物相互作用
作用减弱
可降低普利类药物、塞米类药物、噻嗪类药物和布美他尼、依他尼酸、氨噻酮、帕胺类、美托拉宗、吡咯他尼、喹乙宗等药物的降压利尿作用。
可减弱阿米洛利、坎利酸钾、螺内酯、氨苯蝶啶的利尿作用,并使血钾升高和使肾中毒。
可降低地平类药物、地尔硫草、氟桂利嗪、利多氟嗪、加洛帕米、维拉帕米的降压作用,增加胃肠道出血风险。
作用损害
不良反应增加:与丙磺舒合用,该药血药浓度升高,不良反应随之增加;与酮洛酸合用可增加该药不良反应发生率;与NSAID合用,不良反应增多,并有致溃疡发作的危险。
胃肠道和肾脏损害:饮酒增加胃肠道不良反应发生率;与蚂蝗合用可增加胃黏膜损伤;与β-葡聚糖合用可导致严重胃肠道损害;与他克莫司合用有导致急性肾衰竭的报道;与黑叶母菊合用有增加胃肠与肾脏不良反应的风险;与肝素及双香豆素等抗凝药同用,出血时间延长,可出现出血倾向,并有导致胃肠道溃疡的可能。
其他损害:与口服降糖药合用有发生低血糖风险;与有抗凝血作用的药物合用可增加出血的倾向;与达那帕特合用可增加出血和椎管内麻醉血肿的发生率。与氧氟沙星类合用可增加癫痫发生率。
其他
特殊人群用药
有凝血机制或血小板功能障碍、哮喘、心功能不全或高血压、肝和肾功能不全、活动性胃肠出血或活动性消化道溃疡以及老年人均慎用。
禁忌症
注意事项
风险提示
降低阿司匹林药效:2006年9月,美国食品药品监督管理局(FDA)发布警告,称布洛芬可能降低低剂量阿司匹林(81mg/天)的抗血小板作用,使其在心脏保护和预防中风方面的作用减弱。也至少有一项研究提示,当超出非处方用量的萘普生与阿司匹林伍用时,可能会影响到阿司匹林的抗血小板活性。由于其他非选择性OTC非甾体抗炎药也可能对低剂量阿司匹林的抗血小板作用产生影响,故应对该类药物加以考察,除非证明该类药物没有这一效应。对于高危人群,医生应处方对低剂量阿司匹林抗血小板效应没有影响的镇痛药。
引起固定性药疹:2017年10月,中国国家药品监督管理局提示,磺胺类药,非甾体抗炎药、抗肿瘤药、抗菌药物、镇静催眠药及其复方制剂可引起固定性红斑药疹。
导致胎儿肾脏问题:2020年10月15日,美国食品药品管理局(FDA)发布信息,警示在孕20周或之后使用非甾体抗炎药(NSAIDs)可导致罕见且严重的胎儿肾脏问题,可能引起宫内羊水不足并出现并发症。停用NSAIDs后羊水过少的情况通常可逆,但不总是可逆。羊水过少的并发症可能包括胎儿肢体挛缩和肺成熟迟缓。在一些新生儿肾功能受损的上市后报告中,新生儿需要接受侵入性手术,如换血或透析。之后,加拿大卫生部(HealthCanada)也通过一项安全审查,确认从怀孕约20周或之后开始使用非甾体抗炎药,可能会导致未出生婴儿罕见但严重的肾脏问题,并可能导致羊水过少和其他可能的并发症,例如在新生儿中引发肺发育受损和关节运动功能丧失(肢体挛缩)。并建议消费者在怀孕20-28周时不要使用非甾体抗炎药,除非主管医务人员建议这样做。在怀孕最后3个月(即超过28周至妊娠结束),仍禁止使用非甾体抗炎药。
历史
20时间70年代,Harrison等人为了开发更有效和安全的抗炎药物,对不含氮,含有芳基乙酸以及某些芳基取代的烯醇和酚结构特征的化合物进行了大鼠胃水肿以及解热试验,结果发现2-萘乙酸的生物活性最显著。他们又将2-萘乙酸作为先导化合物,合成了一批6-取代的2-萘烷基羧酸,对这些化合物的初步药理学评估表明d-2-(6′-甲氧基-2′-萘)丙酸的抗炎镇痛和解热作用显著,而这就是萘普生。1971年,Roszkowski等人又通过动物实验证明萘普生具有高效的消炎止痛退热作用。
使用情况
萘普生最早由美国辛迪斯(Syntex)公司推出,于1972年在墨西哥上市,1973年在英国上市,1976年在美国上市,随后在全世界许多国家相继上市。萘普生制剂上市后,其销售额平均每年以10.4%的速度递增。1981年,萘普生全球销售额为2亿美元,1984年达到3.2亿美元。1985年,萘普生在美国非甾体类抗炎药物销售榜中占据首位。1988年,萘普生全球销售额达到5亿美元,1992年突破10亿美元,成为继布洛芬之后又一年销售额突破10亿美元大关的解热镇痛药。1994年,由于萘普生良好的疗效和较轻微的不良反应,美国、英国等许多国家相继批准其为非处方药。中国也于2001年将萘普生列入《非处方药品目录》中,包括片剂、胶囊剂、颗粒剂、栓剂、缓释剂等7种剂型的制剂。同时,萘普生也被收入中国《国家基本医疗保险药品目录》中。
该药也可作为兽药,用于缓解炎症。如对马肌肉骨骼系统的其他软组织疾病和肌炎所引起的跛行而导致的疼痛有一定作用;也可为犬治疗骨关节炎和其他的肌肉骨骼系统的炎症疾病,但因为很难准确定量给予萘普生和可能引起不良反应,只有经医生许可,且较安全的NSAIDs药物无效时才考虑将其用于犬;此外,还可用于用于兔/啮齿动物/小型哺乳动物的化脓性关节炎痛。
化学信息
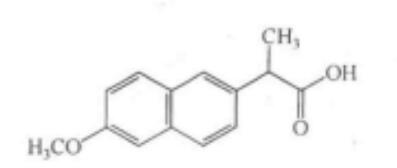
萘普生的化学信息 |
中文化学名 | (+)-(S)-α-甲基-6-甲氧基-2-萘乙酸 |
IUPAC名 | (2S)-2-(6-methoxynaphthalen-2-yl)propanoicacid |
cas号 | 22204-53-1 |
相关cas号 | 26159-34-2(钠盐) |
外观 | 白色至类白色结晶粉末 |
味道 | 几乎无味 |
分子式 | C14H14O3 |
摩尔质量/分子量 | 230.26g/mol |
熔点 | 153-158°C |
溶解性 | 不溶于水;溶于乙醇、无水乙醇和三氯甲烷;略溶于乙醚 |
专利
1970年8月,美国辛迪斯制药公司(SYNTEX CORP)申请了萘普生的专利权(DE2039639A1)“2-(6-Methoxy-2-naphthyl) propionic acid prepns. -anti-pyretics,analgesics,anti-inflammatoryagents”,于1971年4月获得授权,于1993年12月到期。
注释
[a]生物半衰期(t1/2):指药物自体内消除一半(或药物浓度减少50%)所需的时间。
[b]达峰时(tmax):血药浓度达到最大值所需的时间。
[c]FDA药物安全性分级为B:指动物生殖研究未发现药物对胎仔有害,但缺乏人类妊娠期的对照研究。或动物研究发现对胎仔有害(危害程度小)而在人类妊娠研究中未得到证实。
[d]FDA药物安全性分级为D:指有肯定的证据显示对人类胎儿有危险性,但在某些情况下,例如抢救生命或必需治疗但又无其他可代替的药物,此类药物对于妊娠妇女的益处大于对胎儿的危害时才可使用。