简介
盐酸麻黄碱口服、注射很快被吸收,大部分以原形自尿排出。盐酸麻黄碱不良反应包括:偶有鼻刺痛感、烧灼感等局部刺激症状;偶有患者使用后出现血压升高等。药物大剂量或长期使用可引起精神兴奋、震颤、焦虑、失眠、心悸、心动过速等反应。妊娠期妇女慎用。不同药物联合使用时,需要注意药物间相互作用关系。
盐酸麻黄碱常见剂型为注射剂、滴鼻剂、片剂,其中盐酸麻黄碱注射液、盐酸麻黄碱滴鼻液已纳入国家医保,为医保甲类。
医学用途
适应证
滴鼻剂:用于急、慢性鼻炎、鼻窦炎,缓解鼻黏膜充血肿胀引起的鼻塞,减少鼻腔分泌物。也用于鼻出血辅助治疗。
片剂:可用于慢性低血压症;缓解荨麻疹和血管神经性水肿等过敏反应。也可缓解支气管哮喘的发作,倾向少用。
注射剂:用于蛛网膜下腔麻醉或硬膜外麻醉引起的低血压症及慢性低血压症。
用法与用量
鼻部用药:成人:滴鼻或喷入鼻腔,用1%溶液,一日3次,一次3~4滴;止血用2%的溶液。儿科:滴鼻或喷入鼻腔,用0.5%浓度,一次3~4滴,一日3次。
慢性低血压:每次口服25-50mg,每日2~3次。
支气管哮喘:口服常用量,成人每次15-30mg,每日3次;极量:成人口服每次60mg,每日150mg。
注射剂常用量:皮下或肌内注射每次15-30mg,每日3次;极量:皮下或肌内注射每次60mg,每日150mg。
制剂与规格
药品名称 | 制剂 | 医保类型 | 规格 |
盐酸麻黄碱注射液 | 注射剂 | 甲类 | 1ml:30mg |
盐酸麻黄碱滴鼻液 | 滴鼻剂 | 甲类 | 1% |
盐酸麻黄碱片 | 片剂 | - | 15mg;25mg;30mg |
药理机制
鼻部用药:该药物通过激动α受体引起血管收缩,从而减少鼻腔黏膜容积。其血管收缩作用比较持久而缓和,对鼻黏膜上皮纤毛活动影响少,改善鼻腔通气,促进鼻窦引流,并可减轻局部炎症。
临床用药:该药可直接激动肾上腺素受体,也可通过促使肾上腺素能神经末梢释放去甲肾上腺素而间接激动肾上腺素受体,对α-和β-受体均有激动作用。可舒张支气管并收缩局部血管,其作用时间较长;加强心肌收缩力,增加心输出量,使静脉回心血量充分;有较肾上腺素更强的兴奋中枢神经作用。
药代动力学
口服很快被吸收,皮下注射吸收比口服快,可通过血脑屏障进入脑脊液。
风险与禁忌
不良反应
偶有鼻刺痛感、烧灼感等局部刺激症状。
高浓度、频繁和长期使用,对鼻黏膜有损害作用,长期使用可致药物性鼻炎。
偶有患者使用后出现血压升高。
对前列腺肥大者可引起排尿困难。
药物过量
大剂量或长期使用可引起精神兴奋、震颤、焦虑、失眠、心悸、心动过速等反应。
药物相互作用
与肾上腺皮质激素合用,可增加它们的代谢清除率,须调整皮质激素的剂量。
尿碱化剂,如抗酸药、钙或镁的碳酸盐、枸橼酸盐、碳酸氢钠等,影响该药品在尿中的排泄,延长该药品的t1/2及作用时间,可致麻黄碱中毒。
与α受体阻断药如酚妥拉明、哌唑嗪、妥拉唑林及酚噻嗪类药合用时,可对抗该药品的升压作用。
与全麻药如氯仿、氟烷、异氟烷等同用,可使心肌对拟交感胺类药物反应更敏感,有发生室性心律失常危险,必须同用时,该药品用量应减小。
与三环类抗抑郁药如马普替林同用时,降低该药品的升压作用。
与洋地黄苷类合用,可致心律失常。
与麦角新碱、麦角胺或催产素同用,可加剧血管收缩,导致严重高血压或外围组织缺血。
与多沙普仑同用,两者的升压作用均可增强。
特殊人群用药
妊娠期妇女慎用。
儿童不宜长期使用。
注意事项
不宜长期使用,建议使用5~7天。
有交叉过敏反应,对其他拟交感胺类药,如肾上腺素、异丙肾上腺素等过敏者对该药品也过敏。
如有头痛、焦虑不安、心动过速、眩晕、多汗等症状,应注意停药或调整剂量。
短期内反复用药,作用可逐渐减弱(快速耐受现象),停药数小时后可以恢复。每日用药如不超过3次,则耐受现象不明显。
甲状腺功能亢进、高血压、动脉硬化、心绞痛等患者禁用。
风险提示
国家药品监督管理局发布药物警戒快讯 2007年第5期(总第36期),提示英国就限制含伪麻黄碱和麻黄碱药品的销售公开征询意见 :2007年3月7日,英国药品和健康产品管理局(MHRA)发布征求意见函,就从法规层面上限制含伪麻黄碱和麻黄碱药品的销售(如将非处方药转为处方药)问题广泛征求业界和患者的意见。
历史
1885年,日本化学家山成(Yamanashi G.)首先从麻黄Ephedra sinica中分离出不纯净但有类似麻黄活性的组分。
1887年,日本化学家长井(Nagai N.)分离出一种纯净的碱性物质,命名为麻黄碱。
1922年,德国科学家埃姆德(Emde H.)等研究表明,麻黄喊的化学结构为2-甲胺基-1-苯基-1-丙醇,含两个不对称碳原子;并观察到麻黄碱和伪麻黄碱在回流的盐酸中可相互转化,确定两者互为非对映异构体。
从1924年开始,中国药理学家陈克恢连续在国际上发表了其在L-麻黄碱药理学上的研究成果,揭示了L-麻黄碱的基本药效作用,为中药药理学的开创及肾上腺素受体激动药和阻断药的发展做出了重要贡献。
1927年,盐酸麻黄碱被用于治疗小儿哮喘。
1950年,英国科学家布儒斯特(Brewster P.)等通过化学方法将麻黄碱的构型与(R)-(-)-扁桃酸和L-丙氨酸的构型相关联,从而确定了麻黄碱和伪麻黄碱的构型。
使用情况
1927年1月,日本制药商日医工株式会社(Nichi-Iko Co., Ltd.)获批上市麻黄碱注射液40mg,商品为麻黄碱“永井”注射液(ヱフェドリン「ナガヰ」注射液)。
1990年6月27日,英国制药公司SNIGD(UK Limited)首次获批上市盐酸麻黄碱片BP60mg,并于2006年10月6日10再次获批继续生产盐酸麻黄碱片。
1996年12月3日,法国莱格拉斯实验室(Laboratoires LEGRAS)获批生产盐酸麻黄碱喷雾鼻用溶液。
2020年12月1日,中国吉林省利华制药有限公司获批生产盐酸麻黄碱片,批准文号为国药准字H22022755,规格为25mg,剂型为片剂。
化学信息
化学名称:[R-(R,S)]-α-[1-(甲氨基)乙基]苯甲醇盐酸盐
化学结构式:
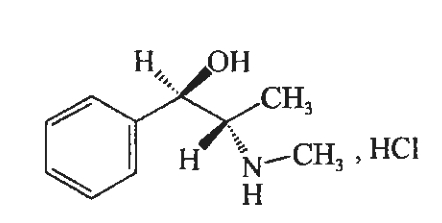
分子式:C10H15NO•HCl
分子量:201.70
熔点:217~220°C
性状:该药为白色针状结晶或结晶性粉末;无臭。
水溶性:该药在水中易溶,在乙醇中溶解,在三氯甲烷或乙醚中不溶。
比旋度:取该药,精密称定,加水溶解并定量稀释制成每1ml中约含50mg的溶液,比旋度为-33°至-35.5°。
专利
美国礼来公司在1928年7月21日对麻黄碱申请了发明专利,申请号:US19280294585,并于1931年3月31日获得授权。
易制毒化学品管理
盐酸麻黄碱、麻黄素是制毒的重要原料,已被纳入易制毒化学品管理。
根据《易制毒化学品管理条例》的规定,盐酸麻黄碱滴鼻液为药品类易制毒化学品单方制剂,只能由麻醉药品定点经营企业经销,且不得零售。
根据《关于印发药品类易制毒化学品专项整治行动实施方案的通知》国食药监电[2012]38号)和《关于加强含麻黄碱类复方制剂管理有关事宜的通知》(国食药监办[2012]260号)的要求,麻黄碱含量超过30mg的复方制剂已从非处方药转为处方药管理。