简介
盐酸舍曲林片常见的不良反应有腹泻、便秘、畏食、消化不良、心悸、震颤、头晕、失眠、嗜睡、多汗、口干、性功能障碍等。少见不良反应有血清氨基转移酶升高低钠血症、高血压、低血压、心动过速、心电图异常、体重改变、静坐不能、痛经、闭经等。对舍曲林过敏、严重肝肾功能不全和使用单胺氧化酶抑制药的患者禁用。
盐酸舍曲林片为片剂,规格多为25mg/片或50mg/片(按舍曲林计)。口服给药,为处方药物,已纳入中国国家医保目录(乙类)。
医学用途
适应证
盐酸舍曲林用于治疗抑郁症、强迫症、创伤后应激障碍(PTSD)、经前期紧张症(PMDD)、社交焦虑障碍及FDA批准的其他适应证。
用法用量
口服,一日有效剂量为50mg。疗效不佳者可增加剂量,最大为一日200mg。长期用药应维持在最小有效治疗剂量。肝肾功能不全者应适当减小剂量。
口服,6-12岁儿童,起始剂量次25mg,一日1次。13-17岁少年,起始剂量一次50mg,一日1次。如需要,至少间隔1周,增加25~50mg,最大剂量一日200mg。单次服用,早服或晚服均可。
制剂与规格
25mg或50mg/片(按舍曲林计)。
药理机制
盐酸舍曲林片为选择性5-羟色胺(5-HT)再摄取抑制药。通过选择性抑制5-HT的再摄取,增加突触间隙5-HT浓度,从而增强中枢5-HT能神经功能,发挥抗抑郁作用。舍曲林还抑制缝际区5-HT能神经放电,由此增强蓝斑区的活动,导致突触后膜β受体与突触前膜α2受体的低敏感化。盐酸舍曲林与毒蕈碱、肾上腺素、y-氨基丁酸、苯二氮䓬类受体无亲和力。动物实验未发现盐酸舍曲林具有兴奋、镇静、抗胆碱作用和心脏毒性。
药代动力学
盐酸舍曲林片口服吸收缓慢,达峰时间为4.5~8.4小时,有首关代谢。蛋白结合率高达98%。体内分布广,可进入乳汁。在肝脏代谢,生成失活的N-去甲基舍曲林,进一步与葡糖醛酸结合。代谢产物从尿和类便等量排出。半衰期为22一36小时。每日服药1次,1周后达稳态浓度。
风险与禁忌
不良反应
常见不良反应有恶心、腹泻、便秘、畏食、消化不良、心悸、震颤、头晕、失眠、嗜睡、多汗、口干、性功能障碍等。
少见不良反应有血清氨基转移酶升高、低钠血症、高血压、低血压、心动过速、心电图异常、体重改变静坐不能、痛经、闭经等。
偶见不良反应有凝血障碍、水肿、轻度躁狂、精神运动性兴奋、癫痫发作、溢乳、男性乳房增大、呼吸困难、阴茎异常勃起、皮疹、脱发、光过敏反应、自杀意念等。
药物相互作用
与单胺氧化酶抑制药合用可出现5-HT综合征。停用单胺氧化酶抑制药14天后才可用,同样,停用14天以上才可用单胺氧化酶抑制药。
盐酸舍曲林能抑制细胞色素氧化酶2D6(CYP2D6),与经CYP2D6代谢的药物合用时,可产生药物相互作用,导致不良反应。
与锂盐合用时可能产生药效学的相互作用,出现震颤,应谨慎。
与其他能增强5-HT能神经功能的药物(如氯米帕明、阿米替林、丙米嗪、苯丙胺、芬氟拉明等)合用时,可导致5-HT综合征。
与茶碱合用时,使后者的血药浓度升高,增加茶碱不良反应的发生。
盐酸舍曲林能抑制苯妥英钠的代谢而增加后者的毒性。
利福平等CYP诱导药可加速盐酸舍曲林代谢,使血药浓度和疗效降低。西咪替丁等CYP抑制药可减慢盐酸舍曲林代谢,升高血药浓度,产生不良反应。
与乙醇合用,可使精神和运动技能损害的危险性增加。
与血浆蛋白结合率高的药物合用时,可能存在潜在的药物相互作用。
与华法林合用时可延长凝血酶原时间,需注意。
特殊人群用药
儿童
在儿童和青少年抑郁症和其他精神障碍中的短期研究发现,抗抑郁药会增加自杀意念和自杀行为(自杀)的风险。如果考虑给儿童和青少年使用该药物,必须权衡这种风险与临床的实际需要。对于已经用药的患者,应密切观察可能的临床症状恶化、自杀和异常的行为改变。
老人
老年人血浆清除率下降,应减量。
妇女
哺乳期妇女不宜使用。美国FDA妊娠期药物安全性分级:口服给药C。
禁忌
对舍曲林过敏、严重肝肾功能不全和使用单胺氧化酶抑制药的患者禁用。
注意事项
有癫痫史、双相情感障碍、近期发生心肌梗死、心脏疾病、肝肾功能不全、血小板聚集功能受损、血容量不足或使用利尿药者慎用。
虽然研究显示舍曲林对精神运动性活动没有影响,但从事驾驶及操作机械等具有潜在危险性工作的患者仍应慎用。
不应与单胺氧化酶抑制药合用,否则可出现严重的甚至致命的不良反应。
慎用于正在服用非甾体抗炎药(NSAID)、阿司匹林或其他抗凝药的患者,可能引起出血。
风险提示
2008年2月4日,英国药品和健康产品管理局(MHRA)发布关于修改抗抑郁药说明书的信息,警告25岁以下成年患者使用抗抑郁药(含舍曲林)导致自杀风险升高。
2011年10月20日,美国食品药品监督管理局(FDA)更新利奈唑胺或亚甲兰与血清素能抗精神病药相互作用的安全性信息,提示在FDA药品不良事件报告系统中与利奈唑胺或亚甲蓝有相互作用的SSRI药物有帕罗西汀、氟伏沙明、氟西汀、舍曲林、西酞普兰、依他普仑和维拉佐酮。
2020年6月22日,欧洲药品监督管理局(EMA)药物警戒风险评估委员会(PRAC)发布信息,警示舍曲林显微镜下结肠炎的风险。
2020年10月26日,欧洲药品监督管理局(EMA)发布消息,警示使用舍曲林有产后出血风险。
历史
在20世纪70年代初,美国辉瑞公司的化学家莱因哈德·萨基(Reinhard Sarges)基于抗精神病药氯氟噻嗪(chlorprothixene)和thiothixene的结构发明了一种新的精神药物命名为他美曲林(Tametraline)。这种药物是一种去甲肾上腺素和较弱的多巴胺再摄取抑制剂,但在动物实验中观察到不良的刺激作用,因此他美曲林(Tametraline)的研究很快就被停止了。
1977年,辉瑞公司药理学家肯尼斯(Kenneth)对他美曲林(Tametraline)产生了兴趣,于是和化学家威拉德·韦尔奇(Willard Welch)合作以他美曲林(Tametraline)为基础,开发衍生物合成了一些有效的去甲肾上腺素和三胺再摄取抑制剂。然而,他们意外地发现其中有一种无作用的顺式结构是5HT的再摄取抑制剂。经过一系列的改进和动物实验,他们找到了最有效和选择性的异构体,最终将其命名为舍曲林。
使用情况
舍曲林由美国辉瑞公司在20世纪90年代初开发,1990在英国上市,1991年12月获得FDA批准,1992年在美国上市。
1995年,中国开始进口盐酸舍曲林原料及片剂,同年在法国、德国、日本等国家上市。
1998年2月,中国批准大连辉瑞制药厂生产盐酸舍曲林片剂(进口原料分装),商品名为左洛复。此后,中国先后有 10 多家企业获得舍曲林片剂及胶囊剂的生产批文。
化学信息
化学名称
(1S-顺式)-4-(3,4-二氯苯基)-1,2,3,4-四氢-N-甲基-1-萘啶胺盐酸盐。
化学结构式
分子式:C17H17NCl2·HCl
分子量:342.7
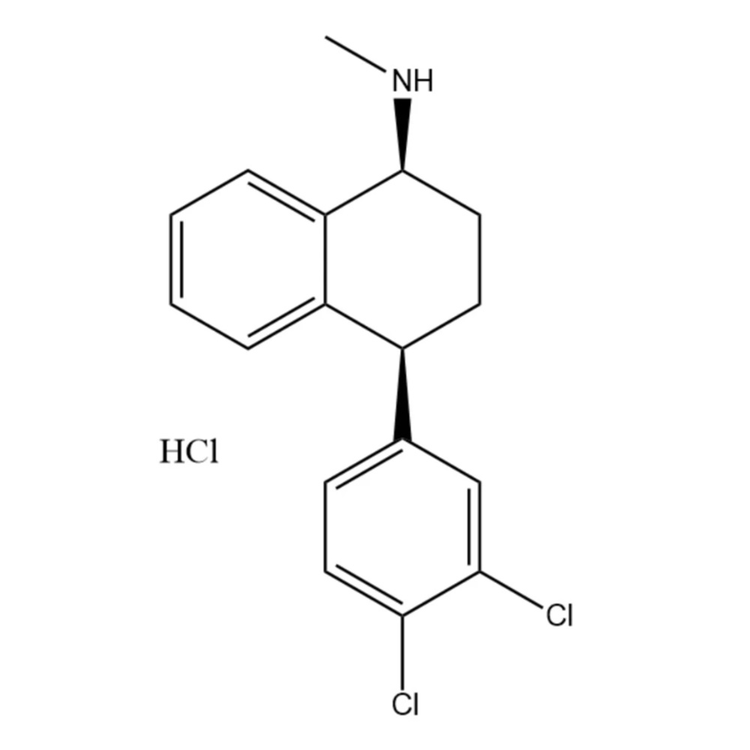
参考资料:
专利
辉瑞公司分别于1981年和1985年对盐酸舍曲林的制备方法申请了欧洲专利和美国专利,专利号分别为Eur.Pat.Appl.30.081和U.S.Pat.4,536,518。1996年12月25日爱尔兰辉瑞公司的郁乐复在中国获准行政保护,授权号为B-E96122516,法定授权保护期自授权之日起7年6个月。
注释
[a]药物首次通过肝时即被代谢一部分,使进入体循环的药量减少,药效降低,这种现象称为首关代谢。
[b]美国FDA妊娠期药物安全性分级有5类。A类:已证实药物对胎儿无不良影响。B类:动物试验及人类均未证实对胎儿有危害(动物试验对胎仔无危害但未有对人类研究的报道)。C类:对动物及人类均无充分的研究,或对动物胎仔有不良影响,但未见人类有关的报道。D类:对胎儿有危害的迹象,但治疗孕妇疾病的效益明显地超过药物的危害。X类:证实对胎儿有害,妊娠期禁用的药物。