简介
不良反应对于肝功能、免疫系统、泌尿系统、肌肉骨骼组织以及精神异常:包括攻击性倾向的精神病行为,可能增加心脏相关死亡风险。不良反应大多轻微,具有自限性。该药禁用于正在接受硫唑嘌呤、巯嘌呤治疗的患者。儿童用药的安全性和有效性尚不明确,老年人与年轻患者用药的安全性和有效性不存在有临床意义的差异,妊娠和哺乳期妇女慎用该药,FDA(美国食品药品监督管理局)对非布司他的妊娠安全等级分级为C级。2016年,加拿大卫生部发现该药对已有心血管疾病和(或)风险因素患者可能增高心力衰竭风险。2019年,FDA发布信息,警告抗痛风药非布司他可能增加患者死亡的风险,并要求限制非布司他的使用。2019年,加拿大卫生部发布信息,将通过致医务人员信函方式警示非布司他增加心血管死亡风险。
非布司他性状为白色结晶性粉末,易溶于二甲基甲酰胺、溶于二甲亚砜,几乎不溶于水,难溶于乙醇,微溶于甲醇、乙腈。处方药,已纳入中国国家医保乙类。
医学用途
适应证
适用于痛风患者高尿酸血症的长期治疗,不推荐用于无临床症状的高尿酸血症。
用法用量
口服。推荐 40 mg或 80 mg一日一次,起始剂量为 40 mg,一日一次。如果 2周后,血尿酸水平仍不低于 6 mg / 100 ml(约 360μmol/L),建议剂量增至 80 mg,一日一次。
制剂与规格
非布司他片:40 mg;80 mg;120mg。
药理机制
该药为 2-芳基噻唑衍生物,是一种黄嘌呤氧化酶抑制剂,通过抑制尿酸合成降低血清尿酸浓度。非布司他常规治疗浓度下不会抑制其他参与嘌呤与嘧啶合成与代谢的酶。
药代动力学
在健康受试者中,10~120 mg剂量范围内,单次和多次给药,非布司他的最大血浆浓度(Cmax)和AUC(药时曲线下面积)呈剂量相关性增加。每 24 小时给予治疗剂量时,体内无蓄积。非布司他半衰期(t1/2)约为5~8小时。通过群体药代动力学分析,非布司他在痛风的高尿酸血症患者中的药代动力学参数与健康受试者相似。口服给药后,放射性标记的非布司他的吸收率至少为 49%(根据尿液中总回收的放射性标记物)。服药后1~1.5小时能达到最大血浆浓度。多次口服非布司他40mg/d或80mg/d,Cmax分别是(1.6±0.6)μg/ml,(2.6±1.7)μg/ml。
风险与禁忌
不良反应
药物过量
对健康受试者给药该药剂量达到每日300mg,持续7日,无剂量限制性毒性。尚无临床药过量的病例报告。药物过量患者应进行对症和支持疗法。
药物互相作用
特殊人群用药
肝、肾功能不全患者:轻中度肝肾功能不全者无需调整剂量,尚未进行重度肝肾功能不全者使用该药的疗效及安全性研究,应慎用。
儿童:18 岁以下儿童用药的安全性和有效性尚不明确。
老年人:65 岁及以上老人与年轻患者用药的安全性和有效性不存在有临床意义的差异,但不排除部分老年人对该药具有更高的敏感性。
妊娠期妇女:美国FDA(美国食品药品管理局)对非布司他的妊娠安全等级分级为C级,尚无妊娠期妇女用药充分严格的对照研究资料,仅在利大于弊时方可使用。
哺乳期妇女:哺乳期妇女应慎用该药。如确需使用,应选择停药或停止哺乳。
禁忌
该药禁用于正在接受硫唑嘌呤、巯嘌呤治疗的患者。
注意事项
痛风发作。为预防治疗初期的痛风发作,建议同时服用非甾体抗炎药或秋水仙碱。在非布司他治疗期间,如果痛风发作,无须中止非布司他治疗。应根据患者的具体情况,对痛风进行相应治疗。
心血管事件。用药时注意监测心肌梗死和脑卒中的症状及体征。
肝脏的影响。首次使用非布司他之前患者应该进行一次肝功能测试,将此结果作为基线水平。如果患者被发现有肝功能异常(ALT超过参考范围上限的3倍以上),应该中止服药,并调查以确定可能的原因。
继发性高尿酸血症。不建议将该药应用于尿酸盐大量升高的患者(如恶性疾病、Lesch-Nyhan 综合征)少数病例显示,尿中黄嘌呤浓度明显升高后可在泌尿道沉积。
风险提示
2016年4月1日,加拿大卫生部发布信息称,在发现一些可疑与使用非布司他(Febuxostat)相关的国际心力衰竭病例后,加拿大卫生部进行了一项安全性回顾分析。加拿大卫生部要求非布司他的生产商在其处方信息中纳入一项关于对已有心血管疾病和(或)风险因素患者可能增高心力衰竭风险的声明。
2016年6月13日,加拿大卫生部网站发布信息,公布其对抗痛风药非布司他与DRESS风险的评估结果。已知别嘌呤醇也可引起严重皮肤反应,包括DRESS。许多在使用非布司他时报告严重的皮肤反应和超敏反应的患者此前也报告过别嘌呤醇的皮肤反应。提示DRESS与非布司他之间可能存在关联性,要求非布司他的生产商将DRESS纳入加拿大的非布司他产品说明书信息中。
2019年2月21日,美国食品药品管理局(FDA)发布信息,警告抗痛风药非布司他可能增加患者死亡的风险,并要求限制非布司他的使用。FDA提醒患者,如果有心脏病或中风病史,应告知医生权衡使用非布司他获益与风险。在服用非布司他期间出现胸痛、呼吸急促、心跳过快或不规则、身体一侧麻木或虚弱、头晕、说话困难、突发性剧烈头痛等症状,应立即就医。未咨询医生前不要擅自停药,以免痛风症状恶化。FDA提醒医务人员,非布司他仅用于别嘌醇治疗失败或不耐受的患者,应告知患者注意其心血管风险,出现上述症状立即就医。
2019年11月4日,加拿大卫生部发布信息,将通过致医务人员信函方式警示非布司他增加心血管死亡风险。提醒患者,在服用非布司他的患者中已有心脏病发作、中风和心脏相关死亡的报道。患者如果有心脏病或中风病史,应告知医生。在服用非布司他期间如出现胸痛、晕厥或头晕、加快或不规则心跳、说话困难、视力突然模糊或头痛等心血管疾病症状,应停止服药,并立即就医。
历史
非布司他是二十世纪八十年代年以来,首个通过抑制尿酸合成的抗痛风药,其作用强大,效果明显,为别瞟醇不耐受或者过敏的患者,提供一种更可靠的选择。日本帝人制药公司为本品原研厂家,于2004年初在日本申请上市。2009年2月,非布司他被美国 FDA 批准用于长期治疗伴随痛风的高尿酸血症患者。2013年2月4日,国家食品药品监督管理局( CFDA)首次批准非布司他在中国上市。
使用情况
2004年,非布司他在日本申请上市,日本帝人制药公司为本品原研厂家。
2013年2月4日,杭州朱养心药业有限公司生产的非布司他,被中国国家食品药品监督管理局( CFDA)首次批准在中国上市。
2013年6月26日,江苏万邦生化医药股份有限公司生产的非布司他获批在中国上市。
2013年7月16日,江苏恒瑞医药股份有限公司生产的非布司他获批在中国上市。
2018 年 10 月,中国首次获批准进口非布司他片。
化学信息
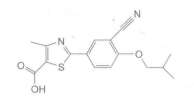
化学名 | 2-(3-Cyano-4-isobutoxyphenyl)-4-methyl-1,3-thiazole-5-carboxylic acid |
分子式 | C16H16N2O3S |
分子量 | 316.37 |
外观 | 白色结晶性粉末 |
溶解性 | 易溶于二甲基甲酰胺、溶于二甲亚砜,几乎不溶于水,难溶于乙醇,微溶于甲醇、乙腈 |
熔点 | 205~208℃ |
CAS | 144060-53-7 |
ATC | M04AA03 |
专利信息
2004年,非布司他片在日本获得专利,专利持有人为日本帝人公司,日本帝人制药公司为该药的原研厂家。
2007年5月30日,非布司他的新晶型及其制备方法在中国获得专利,专利持有人为江苏万邦生化医药集团有限责任公司。