简介
服用异维A酸常见的不良反应有口唇干燥、脱屑,口干,皮肤干燥、脱屑、瘙痒等,少见的反应有精神抑郁、皮肤对日光敏感性增加等,可引起血脂升高,偶见肝、肾功能受损。过量服用可出现呕吐、面部发红、唇干裂、腹痛等症状。妊娠期妇女、哺乳期妇女、儿童禁用。
异维A酸常见剂型为异维A酸胶丸、异维A酸凝胶。异维A酸已纳入国家医保,为医保乙类。
医学用途
适应证
用法与用量
该药物应在医生指导下使用。
口服:一次10~20mg(按体重每日0.5~1.0mg/kg),一日2~3次。一个月后视病情可减为一日1~2次,一次10~20mg,饭后服用。疗程一般为3个月,视病情遵医嘱增减。
局部外用:取适量涂于患处,每晚睡前涂1次。
制剂与规格
异维A酸胶丸:10mg。
异维A酸凝胶:0.05% 10g:5mg。
药理机制
具有缩小皮脂腺,抑制皮脂腺活性,减少皮脂分泌,以及减轻上皮细胞角化和减少毛囊中痤疮丙酸杆菌的作用。内服后,皮肤,尤其是头面部的油脂分泌会明显减少。
药代动力学
口服后迅速由胃肠道吸收,2~4小时达血浓度高峰,药物的消除半衰期为10~20小时,在肝脏或肠壁代谢,以原形及代谢产物由肾脏和胆汁排出。
风险与禁忌
不良反应
口服
常见的有口唇干燥、脱屑,口干,皮肤干燥、脱屑、瘙痒等。
少见的反应有精神抑郁、皮肤对日光敏感性增加、掌跖脱皮、眼干、胃不适、疲乏等。
可引起血脂升高。偶见肝、肾功能受损。
结膜炎、严重者角膜混浊、视力障碍、视盘水肿、头痛、头晕、精神症状、抑郁、良性脑压增高。
毛发疏松、指甲变软。
骨质疏松、肌肉无力、疼痛、胃肠道症状、鼻出血等。
实验室检查可引起红细胞沉降快、肝酶升高、血脂升髙、血糖升高、血小板下降等。
上述不良反应大多为可逆性,停药后可逐渐得到恢复。轻度不良反应,不必停药,可减量使用。
局部外用
常见不良反应为皮肤刺激现象,发红、灼热及脱屑等。
药物过量
过量服用可出现呕吐、面部发红、唇干裂、腹痛、头痛、头昏及共济失调,这些症状能迅速消失而没有明显的后遗影响。
药物相互作用
该药应避免与四环素同时服用。
与阿维A、维胺酯或维A酸类共用,可增加不良反应的发生率及严重程度。
与光敏感药物共用,可发生加剧的光敏反应。
特殊人群用药
妊娠期妇女、哺乳期妇女禁用。
儿童禁用。
禁忌证
肝、肾功能不全者禁用。
高脂血症患者禁用。
维生素A过量禁用,对维A酸类药物过敏者禁用。
注意事项
该药有致畸胎作用,育龄期妇女或其配偶服药期间及服药前、后三个月内应严格避孕。接受治疗前2周应作妊娠试验,以后每月1次,确保无妊娠。
服药期间应定期作血、尿常规、血脂、肝功能等检查。
可发生光敏感反应,在服药期间应避免日晒。
不宜用于皮肤皱褶处,避免接触眼睛和其他黏膜(如口、鼻等)。
糖尿病、肥胖症、酗酒及脂质代谢紊乱者慎用。
风险提示
2017年7月13日,国家药品监督管理局发布的药物警戒快讯2017年第3期(总第167期)中提到“加拿大警示口服异维A酸勃起功能障碍的潜在风险”:加拿大卫生部建议所有异维A酸产品(商品名:Accutane、Clarus和Epuris)均应将勃起功能障碍纳入产品信息的不良反应项中。勃起功能障碍已经出现在Epuris的产品信息中,但尚未出现在其他产品的信息中。
2018年2月7日,国家药品监督管理局发布的药物警戒快讯2017年第12期(总第176期)中提到“英国提示异维A酸罕见的勃起功能障碍和性欲减退风险”:英国药品和健康产品管理局(MHRA)在2017年10月发布信息称,用于治疗严重痤疮的异维A酸口服制剂,收到数例性功能障碍的不良反应报告,主要表现为勃起功能障碍和性欲减退。
2019年12月9日,国家药品监督管理局发布的药物警戒快讯第7期(总第195期)中提到“英国修订口服维A酸类药物的预防妊娠教育材料”:新的处方者检查单、患者提示卡和药师检查单已可获得用于支持服用阿维A、阿利维A酸和异维A酸的妇女实施预防妊娠计划。此外,MHRA对所有口服维A酸类药物的神经精神障碍风险提示进行了统一。
历史
研发背景
痤疮是青少年群体易发的一种慢性炎症性皮肤病,由于该疾病多发生于面部、躯干和背部,并且伴有非炎症性(粉刺)和炎症性(丘疹、脓疱、结节和囊肿)病变,不及时治疗就可能会演变成疤痕,会对生活质量产生负面影响,充分、早期、有效和安全的治疗是病情缓解、无后遗症的关键。
研发过程
自1940年以来,人们就发现维A酸类药物(维生素A及其类似物)可用于治疗多种皮肤病。异维A酸也是一种维A酸类药物,它是由位于美国新泽西州纳特利的霍夫曼罗氏公司(Hoffmann-LaRoche)于20世纪60年代合成。20世纪70年代,担任美国国立卫生研究院(NIH)皮肤病科高级研究员的佩克(Peck)发现异维A酸是治疗严重痤疮的有效药物。于是在1975年,佩克(Peck)联系了霍夫曼罗氏公司(Hoffmann-LaRoche),希望通过口服或外用异维A酸的方式,测试对皮肤病(痤疮、牛皮癣和皮肤遗传性疾病)的治疗效果,以及作为皮肤癌的预防药物。
临床试验
在1977年,佩克(Peck)开始了一项为期四个月的安慰剂对照、双盲临床试验,测试异维A酸在治疗难治性痤疮方面的效果,最终大多数患者的严重痤疮被治愈,即使部分未被治愈,但在无需继续治疗的情况下也能够得到长期缓解。 美国食品药品监督管理局(FDA)基于佩克(Peck)开展的异维A酸临床效果进行综合研判后,于1982年批准霍夫曼罗氏公司(Hoffmann-LaRoche)的异维A酸可作为治疗严重痤疮的口服处方药。从那时起,患者能够在疾病早期阶段就接受异维A酸的有效治疗,严重痤疮的病例数量迅速下降。异维A酸已被全世界数百万人使用。佩克(Peck)凭借在皮肤病学领域的突出贡献,获得的众多奖项,包括在2002年荣获皮肤病学领域的最高奖项皮肤病学基金会的发现奖(Discovery Award of the Dermatology Foundation)。
使用情况
1982年5月7日,瑞士霍夫曼罗氏公司(Hoffmann-LaRoche)口服用的异维A酸胶囊获批上市,商品名为“ACCUTANE”。
2002年11月8日,美国迈兰制药公司(MYLAN PHARMS INC)口服用的异维A酸胶囊获批上市,商品名为“AMNESTEEM”。
2003年4月11日,美国梯瓦公司(TEVA PHARMS USA)口服用的异维A酸胶囊获批上市,商品名为“CLARAVIS”。
2011年8月8日,法国Catalent France Beinheim S.A公司口服用的异维A酸胶囊获批上市,商品名为“ISDIBEN”。
2020年11月22日,中国哈尔滨大中制药有限公司获批生产异维A酸原料药,批准文号:国药准字H20013010。
化学信息
化学名称:3,7-二甲基-9-(2,6,6-三甲基-1-环己烯基)2顺-4反-6反-8反-壬四烯酸
化学结构式:
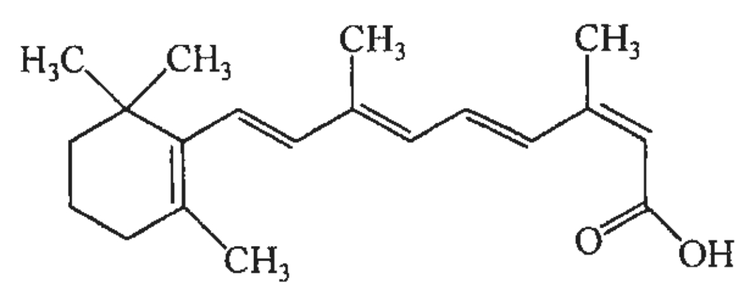
分子式:C20H28O2
分子量:300.44
性状:该药物为黄色至橙黄色的结晶性粉末;对空气、热、光敏感,在溶液中尤为敏感。
水溶性:该药物在三氯甲烷或乙醚中溶解,在乙醇或异丙醇中微溶,在水中几乎不溶。
专利
异维A酸是一种维A酸类药物,霍夫曼罗氏公司(Hoffmann-LaRoche)于1969年获得专利,该专利于2002年到期,异维A酸的仿制药已获得FDA批准并生产,由美国的几家公司以许多不同的名称进行销售。