简介
在自然界中,钠仅以化合物的形式广泛地分布于陆地和海洋中,是地壳中含量排名第六的元素。钠是动植物的必需元素,钠广泛存在于人体肌肉组织和神经组织中,是细胞外液的主要阳离子,起到维持渗透压、维持酸碱平衡、维持神经和肌肉的正常兴奋性的等作用。
由于钠活泼的化学性质,在许多情况下都具有一定的危险性。如钠在遇水或暴露在潮湿空气中会发热,且极易引起燃烧或爆炸。对于钠的消防处理,只能采用干沙或干粉进行灭火。
工业上常用的生产钠的方法是通过电解熔融氯化钠制备。钠广泛用于化工生产、照明行业、电池行业和钢件淬火中。
发现历史
1807年,英国化学家汉弗里·戴维(Humphry Davy)通过电解熔融氢氧化钠首次分离获得了质地柔软的银白色钠。相关化学反应方程式如下:
晶体结构
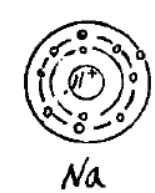
钠晶体属于金属晶体,钠原子之间以金属键相互作用。钠的晶胞中含有2个钠原子,分别位于晶胞中的原点和体心。
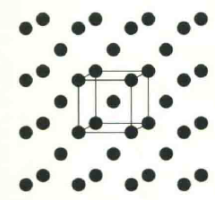
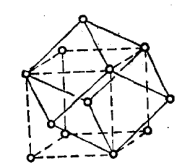
钠晶体为体心立方结构,每个钠原子周围都含有8个相邻的钠原子,这8个钠原子形成一个平行六面体结构单元,只包含一个钠原子。
理化性质
物理性质
通常情况下,常温下的钠为质地软、轻、蜡状且伸展性极好的银白色金属固体,20 ℃时的密度为971 kg/m³,熔点为97.81 ℃,沸点为881.4 ℃,可溶于液氨、汞,不溶于苯、石脑油、煤油。在干燥空气中钠可在>115 ℃的温度条件下发生自燃。钠的临界点为2299.85 ℃、35.46 MPa,其熔化热和汽化热分别为113.5 kJ/kg和4212 kJ/kg,327 ℃时的蒸气压为0.042 mmHg。
钠是优良的导热体和导电体,具有良好的导磁性,同时也具有良好的延展性;钠因其质地柔软可用小刀切割,其新切面有银白色光泽,会在空气中氧化转变为暗灰色,且具有抗腐蚀性。
化学性质
与非金属化合物反应
与水反应
钠的化学性质活泼,在常温或加热时可与水发生爆炸性反应。
检测方法
可采用高氯酸标准溶液滴定法来测定有机酸碱金属盐类物质的含量。以有机碱羧甲基纤维素钠为例,采用冰醋酸作为酸性溶剂,增强其相对碱度,便于强酸性的高氯酸滴定,同时加入一定量的乙酸酐去除水分,以结晶紫为指示剂、高氯酸标准溶液-冰醋酸作为滴定剂,即可测定钠的含量,滴定至溶液显蓝绿色即为滴定终点。
应用领域
化工生产
钠可作为许多化工产品的基础原料,如铅汽油添加剂和石油脱硫剂、氧化剂、漂白剂、农药、催化剂、香料、有机化合物生产用的钠化合物。氨钠法制备的氰化钠、置换氧化钾制备金属钾、还原四氯化钛生产海绵钛。同时还可以作为许多产品的中间体,如氨基钠作为染料靛蓝粉中间体、硼氢化钠、原甲酸三甲酯和甲酸三乙酯等的医药中间体。
照明行业
钠灯是一种气体放电灯,在防腐蚀的玻璃外壳内两端装有电极,抽至真空后加入一定量的钠,通电后钠蒸发,受电子激发的影响即可发出黄光。按照钠蒸气压力的高低可分为低压钠灯和高压钠灯,高压钠灯具有耗电少、寿命长和可以良好的穿透雾气等优点,是机场、码头和高速公路等场所的必要设备。
医药行业
钠可作为制造西力生、维生素和咖啡因等医药产品的制作原料。
钠离子电池
与锂离子电池类似,钠离子电池通过正电荷电子在电极之间的穿梭运动而放电。与锂离子电池相比,钠离子电池可用性更高且成本更低,但钠离子电池较为适用于固定应用场景。钠离子电池属于新一代的化学能源,钠资源丰富,成本低廉分布广泛,具有更高的半电池点位和更加稳定的电化学性能,具有更高的安全性。
钠离子电池的质量重,适用于大型设备能量存储,因此可应用于工业、航天、军事等能量存储领域。钠离子低成本,更使得钠离子电池有望在智能电网及可再生能源的大规模储能中实现广泛的应用。
钢件猝火
熔融钠的冷却能力强。液态钠的温度范围较广,复合钢铁零件热处理所需温度范围,可根据热处理要求适当的选择熔融钠的温度。熔融钠主要用于钢件淬火后的回火,也可用于后续热处理加热,具有热导率高、传热系数高和粘度低等优点。
安全事宜
健康危害
低钠血症
低钠血症可细分为急性/超急性钠血症和慢性低钠血症。
对于急性/超急性钠血症,在血清钠浓度降低至125-130 mmol/L时会出现恶心等不适症状。血清钠降低至115-120 mmol/L则可能会出现头痛、嗜睡、意识模糊、发生痫性发作、昏迷和呼吸停止等生理不适现象,常多发于马拉松运动员、精神病患者或摇头丸使用者。
对于慢性低钠血症,相较于急性低钠血症,患者的脑水肿症状和神经系统症状较轻;临床症状常出现于血清钠含量低于120 mmol/L时会出现乏力、恶心、呕吐、头晕、步态不稳、记忆力下降、意识模糊等临床症状。
高钠血症
高血钠症是在血钠浓度大于145 mmol/L时出现的病理状态,分为急性高容量性高钠血症、慢性高容量性高钠血症、急性低容量性高钠血症、慢性低容量性高钠血症、正常容量性高钠血症、转移性高钠血症六种基本类型。
高钠血症的临床表现取决于血钠浓度升高的速度和程度,急性高钠血症比慢性高钠血症的症状更严重。主要临床表现为神经精神症状包括嗜睡和昏迷。高钠血症的早期主要症状表现为口渴、软弱无力、恶心呕吐等,晚期则会出现脑细胞脱水的相关症状,如烦躁易怒、精神低落、抽搐或癫痫等症状。
泄露应急处理
消防安全
钠在遇水或暴露在潮湿空气中会发热,且极易引起燃烧或爆炸;与碘或乙炔反应剧烈,极易引起燃烧或爆炸。在一定温度下遇四氯化碳在会发生爆炸。
对于有关钠的火灾消防处理,可以采用干沙或干粉进行灭火如干燥氯化钠粉末、干燥石墨粉、碳酸钠干粉、碳酸钙干粉、干沙等灭火。禁止使用水、泡沫、二氧化碳等灭火剂进行灭火。
储存
钠在空气中容易氧化,通常保存在煤油中。储存于阴凉、干燥、通风良好的专用库房内,远离火种、热源。钠需密封包装,不可与空气接触,应与氧化剂、酸类、卤素等分开存放,禁止混存。库房应采用防爆型照明、通风设施,同时禁止采用易产生火花的机械设备和工具,储区应备有合适的材料收容泄漏物。。