相关历史
1663年英国化学家罗伯特·波义耳(Robert Boyle)发现硫化氢可以使银器变黑。1772年瑞典化学家卡尔·威尔海姆·舍勒 (Carl Wilhelm Scheele)证明了硫在氢气中燃烧可以得到硫化氢气体,并且这种气体中的硫,可以用一些氧化剂使其氧化析出;化学家道尔顿曾用实验证明硫化氢是用由元素硫和元素氢组成。1796年化学家贝托雷证明硫化氢不是含氧酸。
在18世纪末,当时化学家在分析各种矿石成分时,是将矿石放入硫酸中加热,此时会放出一种极为难闻的硫磺气(硫化氢)。普罗斯发现这种气体与一些金属盐反应会产生不同颜色沉淀,这个性质的发现便成为新的分析方法的重要依据。1829年德国化学家罗塞科学地制定了以硫化氢为主的系统定性分析。在盐酸处理后的溶液中通入硫化氢,则金、锑、锡、砷、铅、铋、铜、银、汞等离子都形成硫化物的沉淀,从而与其它金属离子分开。这样有步骤地用几种基本的试剂把未知物分为若干组,再分别用特种试剂检验,就可以确定未知物的各成分。所以,硫化氢是分析化学中很重要的基本试剂,在分析化学发展史中,起到了非常重要的作用。
分布来源
硫化氢一般是化学反应和蛋白质自然分解的产物。自然界中硫化氢常含于火山喷射气及矿泉水中,此外动植物以及各种各样的有机垃圾腐烂时都经常产生硫化氢。人们在石油开采、橡胶、鞣革、煤低温焦化、甜菜制糖等生产中有硫化氢产生。在清理水井、下水道、隧道、垃圾堆等作业中,可能遇到。
分子结构

硫化氢的分子结构与水分子相似,分子中的硫采用sp3不等性杂化,分子构型为v形,H-S键长为136pm,键角∠HSH为92°。硫化氢属于极性分子,极性弱于水,分子间不能形成氢键。
理化性质
物理性质
硫化氢为臭鸡蛋气味的无色气体,能与空气混合形成爆炸性气体,易溶于水,常温下,1体积水能溶解约4.7体积硫化氢气体,还可溶于石油、乙醇、二硫化碳、四氯化碳等溶剂。硫化氢的摩尔质量34.08g/mol为,密度为0.92g/cm3,沸点为-60℃,熔点为-85℃,20℃时的蒸气压为1880kPa,空气中的爆炸界限为4.3%~46.0%,自燃温度为260℃。
化学性质
不稳定性
硫化氢被加热至300℃以上会分解为氢气和硫。
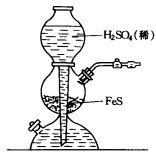
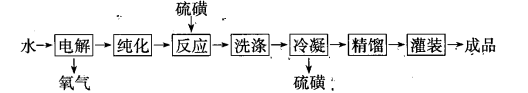
应用领域
化学
硫化氢在分析化学中作为沉淀剂,可以用来分离和鉴定某些金属离子。还可以用来制造多种无机硫化物,如硫化钠、硫氢化钠等,进而用作制造染料、橡胶制品、杀虫剂、塑料助剂、皮革和药物的原料。硫化氢在有机合成中的重要用途是制取硫醇,也是重要的还原剂。
冶金
在冶金工业中硫化氢用于从镍钴矿的浸取液中沉淀硫化铜,从红土的硫酸浸取液中沉淀硫化镍和硫化钴。在核工业中用硫化氢可生产重水。
安全事宜
安全标志
GHS分类
GHS | 危险说明 | 危险等级 |
H220 | 极易燃气体 | 易燃气体 |
H330 | 吸入致命 | 急性毒性,吸入 |
H400 | 对水生生物剧毒 | 对水生环境有害,危害严重 |
相关法规
在我国《职业性接触毒物危害程度分级》(GBZ 230-2010)中规定,把硫化氢定为Ⅱ级(高度危害)。
下表为不同浓度下硫化氢的影响
影响 | 浓度/(mg·m3) | 影响 | 浓度(mg·m3) |
气味的最低阈值 | 0.14~0.28 | 嗅觉麻痹 | 210~350 |
讨厌味有感觉 | 4.2~7 | 引起肺水肿 | 420~700 |
阈限值 | 14 | 窒息 | 700~1400 |
眼睛有害 | 70~140 | 虚脱 | 1400~2800 |
泄露处理
硫化氢发生泄露时,人员应迅速撤离泄漏污染区至上风处,并立即进行隔离(少量泄漏时隔离150m,大量泄漏时隔离300m),严格限制出入并切断火源。应急处理人员需戴自给正压式呼吸器,穿防毒服,从上风处进入现场并尽可能切断泄漏源。同时合理通风,加速扩散,可喷雾状水稀释、溶解,构筑围堤或挖坑收容产生的大量废水。如有可能,将残余气或漏出气用排风机送至水洗塔或与塔相连的通风橱内,或使其通过三氯化铁水溶液,管路装止回装置以防溶液吸回。漏气容器要妥善处理,修复、检验后再用。
消防处理
硫化氢发生火灾时,消防人员必须穿戴全身防火防毒服,切断气源,若不能立即切断气源,则不允许熄灭正在燃烧的气体。喷水冷却容器,可能的话将容器从火场移至空旷处。可用雾状水、泡沫、二氧化碳、干粉进行灭火。
健康危害
接触硫化氢气体或液化气体可引起灼伤、严重损害和(或)冻伤。本品有毒,主要经呼吸道吸收而引起全身中毒,是一种化学性室息性气体;是强烈的神经毒物,对黏膜有强烈刺激作用。
急救措施
皮肤接触:立即脱去污染的衣物,用流动清水冲洗,就医。
眼睛接触:立即提起眼脸,用大量流动清水或生理盐水彻底冲洗至少15分钟,就医。
吸入:立即脱离现场至空气新鲜处,保持呼吸道通畅。如呼吸困难,给输氧,如呼吸停止,即进行人工呼吸。
储存
储存于通风、低温、干燥的库房,与硝酸等强氧化剂分开存放。