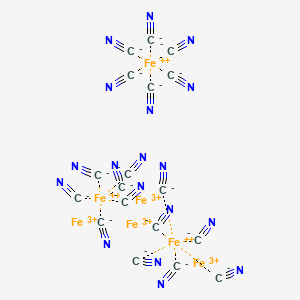
普鲁士蓝,英文名Prussian Blue(简称PB),又名滕氏蓝、亚铁氰化铁,是一种聚合络合物,是由C、N、Fe三种元素组成,一般指亚铁氰化铁,其分子式为Fe₄[Fe(CN)₆]₃,密度为1.8 g/cm³,其不溶于水,微溶于大多数有机溶剂,普鲁士蓝具有立方晶体结构,容易与水形成胶体,因此可以用于作为污水中的吸附剂使用。 其在加热时会分解,可以释放出有毒的氰化氢和氮氧化物的烟雾。普鲁士蓝常被作为颜料在画图和青花瓷器中使用,也应用于雕塑、纺织行业。在医疗、工业、分析化学中也均有应用。
本页面主要目录有关于普鲁士蓝的:研究历史、理化性质、制备方法、应用领域、安全事宜、储存及保藏、结构特点等介绍