相关历史
《唐本草》叙述了氯化铜的制法:“以光明盐、硇砂、赤铜屑酿之为块,绿色。”光明盐就是食盐,用氯化钠、氯化铵和铜屑反应,可生成不纯的氯化铜。李时珍还谈到铜绿的制法:“近时人以醋制铜生绿,取收,晒干,货之。”
19世纪60年代,开发了用氯化铜为催化剂使氯化氢进行氧化以制取氯气的迪肯过程。1959年,人们又发明了乙烯直接氧化法(又称瓦克法),该法以氯化钯一氯化铜一盐酸一水组成的溶液为催化剂,使乙烯直接氧化为乙醛。1978年,日本使用超高分辨力的电子显微镜成功地拍摄了氯化铜——钛花青染料分子结构中的原子照片。
应用领域
工业领域
氯化铜用作电镀槽增加铜离子添加剂;石油工业脱溴、脱硫和纯化剂;金属冶炼;木材防腐;杀虫剂等。
催化剂
氯化铜用作乙烯液相氧化制乙醛、乙烯氯化制二氯乙烷及烃类脱氢等有机合成催化剂。在氯化钯、氯化铜存在下,通过空气将烯烃氧化成醛或酮的过程称为Wacker氧化反应。双键在末端的烯烃氧化成甲基酮。例如:乙烯可以在氯化钯及氯化铜溶液中氧化成乙醛。
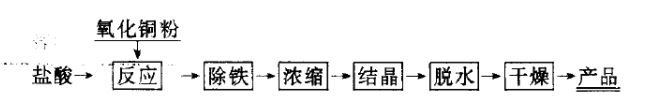
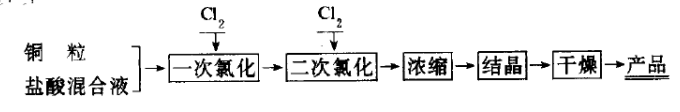
氯化法
通过氯气氧化电解铜粒,制得氯化铜。相关化学反应方程式为:
分子结构
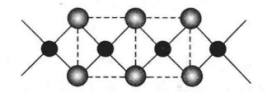
无水氯化铜(CuCl2)具有聚合链式结构,由平面型CuCl4单元共用相对的棱所组成。水合氯化铜(CuCl2·2H2O)结构与无水氯化铜(CuCl2)相似。差异是围绕铜原子的四方平面顶点分别是两个氯原子(两个Cu-CI键)和两个羟基(两个Cu-OH键)。
安全事宜
安全标志
安全标志GHS危害声明GHS | 危险说明 |
H301 | 吞咽有毒(急性毒性,口服) |
H302+H312 | 吞咽或皮肤接触有害(急性毒性,口服;急性毒性,皮肤) |
H302 | 吞咽有害(急性毒性,口服) |
H312 | 与皮肤接触有害(急性毒性,皮肤) |
H315 | 引起皮肤刺激(皮肤腐蚀/刺激) |
H318 | 造成严重的眼睛损伤(严重的眼睛损伤/眼睛刺激) |
H319 | 引起严重的眼睛刺激(严重的眼睛损伤/眼睛刺激) |
H335 | 特异性靶器官毒性,单次暴露;呼吸道刺激 |
H400 | 对水生生物剧毒(对水生环境有害,危害严重) |
H410 | 对水生生物毒性很大,影响持久(对水生环境有害,长期危害) |
H411 | 对水生生物有毒,影响持久(对水生环境有害,长期危害) |
毒性
大鼠经口LD50:140mg/kg。
健康危害
氯化铜对皮肤有刺激作用,粉尘刺激眼睛,并引起角膜溃病。生产人员要穿工作服,戴口罩、手套等劳保用品,生产设备密闭,车间通风良好。下班后要洗淋浴。
急救措施
吸入:呼吸新鲜空气。
摄入:给予大量水;诱导呕吐;就医。
眼睛:用水冲洗15分钟;如果损伤是由固体引起的,就医。
皮肤:用水冲洗。
储存运输
属无机有毒品。应贮存在阴凉、通风、干燥的库房内。注意防潮,不得露天堆放。不可与食用物品共贮混运。运输过程中要防雨淋和日晒。装卸时要小心轻放,防止包装破裂而潮解。