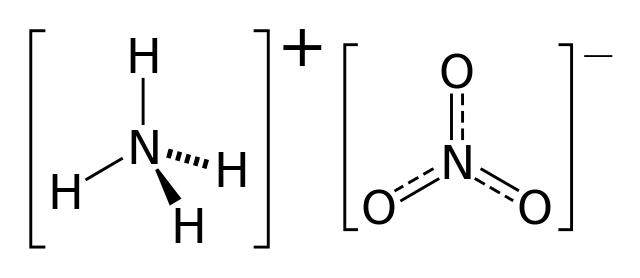发展历史
1659年,德国化学家约翰鲁道夫格劳伯(Johann Rudolf Glauber,1604-1670)首次以氨水和硝酸为原料制备出硝酸铵。约翰鲁道夫格劳伯在1667年-1668年所作的出版物中提到了这种化合物对人类有着十分重要的作用。
1913年,在德国物理化学家弗里茨哈伯(Fritz Haber)和德国化学家卡尔博世(Carl Bosch 1874–1940)的共同努力下氨气的高压合成实现了商业化。同时,巴斯夫工厂(BASF)在德国奥波建立了第一座高压合成氨工厂,极大的促进了合成氨工业的发展。高压合成氨法的出现解决了世界氨资源主要依靠硝石、粪便和焦炭生产,且供应不足的现状。
得益于高压合成氨法的发现,为硝酸铵等含氮产品的生产获得了丰富的原料。自那以后硝酸铵的产率不断上升,被广泛的应用于肥料和炸弹行业。
晶体特点
硝酸铵晶体会随着温度变化发生改性,在169℃-125℃时为稳定的立方晶型I(ε),在84.5℃-125℃时为稳定的四方晶型II(δ),在84.5℃-32℃时为稳定的单斜晶型III(β),在32℃到-16℃时为稳定的斜方六面晶型IV(β),-16℃时为稳定的四面晶型V(α),同时也发现了晶体形态:晶型VI(高于169℃,压力高于9000kg/cm2),晶型VII(低于-170℃)
硝酸铵的一种变体向另一种变体的转变过程时可逆互变异构现象,在当硝酸铵由一种晶体向另一种变体改变的过程中伴随着放热(或吸热),同时,体积、热量、比容、热容和熵都会发生显著的变化。
理化性质
物理性质
硝酸铵室温下为无味白色正交结晶颗粒。硝酸铵极易溶于水,25℃时在水中的溶解度为213g/100g,且溶于水时吸收大量的热;还可溶于醇(甲醇和乙醇)、酸(乙酸和硝酸)、丙酮和氨(液氨、氨水)等中,不溶于乙醚,25℃时的密度为1.72g/cm³,标准大气压下的熔点为169.7°C,20°C时硝酸铵水溶液的蒸气压为2.3kPa。
与其他含氮盐类物质不同,硝酸铵具有高度吸湿性,且吸湿性与温度有很大的关系,一般随温度的升高而大幅度增大,同时由于在不同温度下,硝酸铵在水中溶解度的不同,硝酸铵具有一定的结块性。
化学性质
分解反应
硝酸铵在常温下稳定,不会发生分解反应。而在加热的条件下会发生分解。
在169℃左右加热硝酸铵时,硝酸铵会熔化分解为氨气和硝酸,反应吸收一定热量。
反应方程式为:
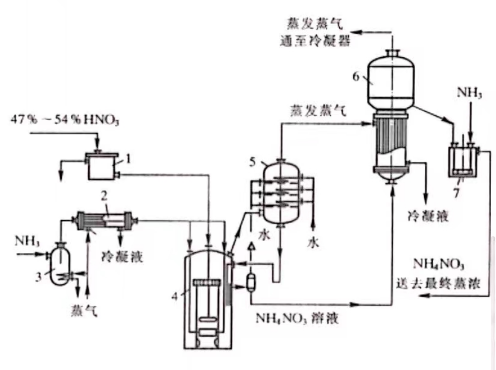
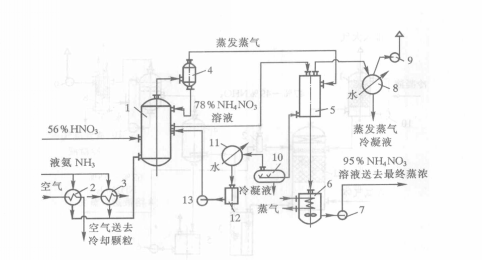
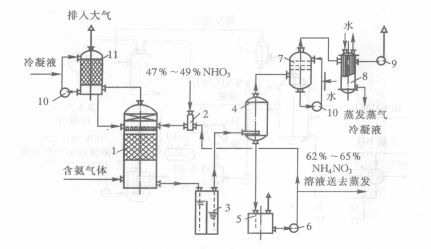
以下为加压中和与真空蒸发中和过程的流程图。
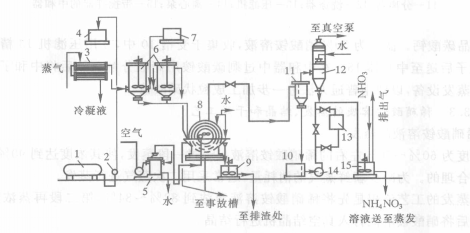
转化法
工艺原理
利用氮磷复合肥生产过程中的副产物Ca(NO₃)₂·H₂O与由NH₃与CO₂制备的(NH₄)₂CO₃反应制备硝酸铵。转换法原理可分为两步,第一步为碳酸铵的制备,第二步为硝酸铵的制备。
其他方法
利用硫酸铵与硝酸钠或硝酸钡发生复分解反应制备硝酸铵。


| 图意 | 氧化性 | 有刺激性 |
GHS分类:
H272(93.72%):可能会加剧火灾;氧化剂(危险氧化性液体;氧化性固体)
H319(97.99%):造成严重眼刺激(警告严重眼损伤/眼刺激)
H335(12.14%):可能引起呼吸道刺激(警告特异性目标器官毒性,单次接触;呼吸道刺激)
毒性
硝酸铵的毒性如下表所示。
实验生物体 | 摄入路线 | 剂量 | 影响 |
大鼠 | 口服 | 2217mg/kg | 致死 |
大鼠 | 口服 | 10mg/kg | 血液:高铁血红蛋白血症-碳氧血红蛋白血症 代谢:体重减轻或体重增加减缓 |
健康危害
储存运输
消防相关
急救措施