简介
氯酸钾是一种极其不稳定的物质,容易分解释放氧气,在酸性介质中,氯酸钾属于强氧化剂,当氯酸钾与碳、硫和某些物质的混合物受到撞击时容易发生爆炸,属于易制爆品。
氯酸钾本身有一定毒性,且燃烧会产生刺激性有毒烟雾,吸入和接触都会对身体造成危害。
利用氯酸钾易释放氧气的性质广泛用于实验室制备氧气,利用氯酸钾的强氧化性,可用作直接滴定剂滴定V³⁺、Sn²⁺和Ti³⁺,同时也用于军事炸药,工业印染,农业肥料,日用烟火等方面。
发现历史
法国著名科学家克劳德路易斯贝尔托莱特(Claude-Louis Berthollet,1748-1822),在1788年使用钾盐(KOH)首次制备出了纯净的钾盐氯酸盐—即氯酸钾。
贝尔托莱特通过将氯气通入热的氢氧化钾水溶液中,结晶出大量钾盐,该盐呈六角形,具有云母光泽。后来贝尔托莱为了验证该盐为含氧的氯盐,将获得的钾盐与木炭混合爆炸,检测爆炸后产物发现仅剩下钾盐氯化物(KCl)。因此,验证这种盐属于“含氧氯钾盐”。贝尔托莱考虑到氯酸钾释放氧气的速度以及它与木炭混合爆炸时的光芒,猜测用这种盐制备的粉末具有一定的特殊性,并在此之后进行了一系列的试验,在某个实验中出现了灾难性的致命爆炸。这一发现对于获得更强大的火药替代硝具有重要意义。
晶体结构
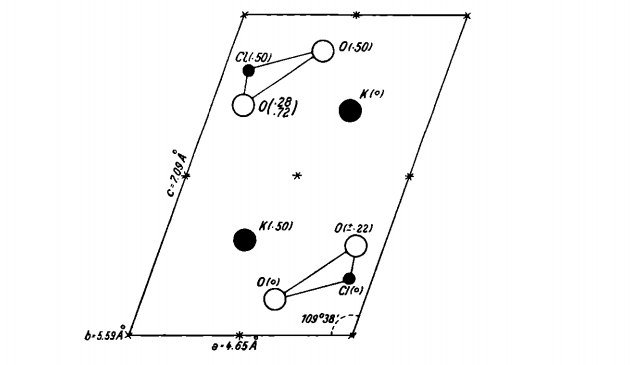
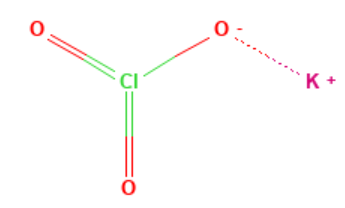
氯酸钾晶体结构属于单斜多面体,其中钾被9个氧原子包围,平均距离为2.94 Å。3个氧原子不对称地位于氯的周围,形成一个ClO₃组。氯酸钾晶体中原子的排列如下图所示。同时氯酸钾具有以c(001)为孪晶面形成孪晶的性质。同时,氯酸钾属于双轴晶体。
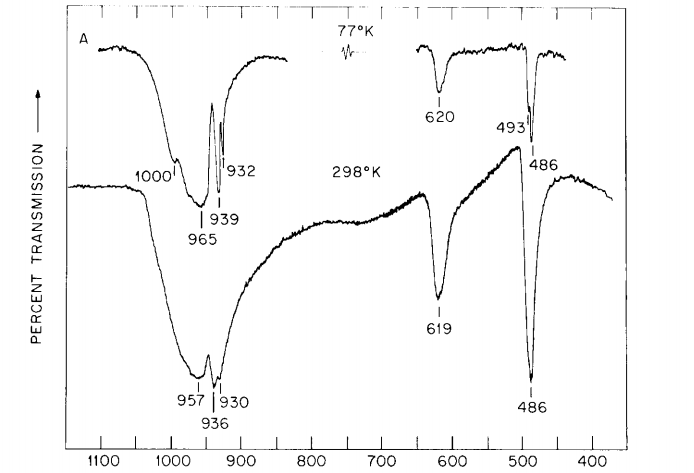
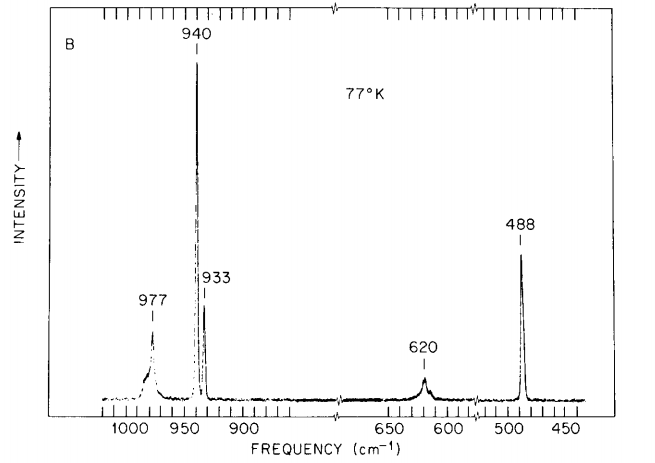
下图为氯酸钾的拉曼光谱多晶和红外光谱。
理化性质
物理性质
氯酸钾常温下为无色、有光泽的晶体或白色颗粒或粉末,其固体无气味,口感清凉,具有咸味。氯酸钾可溶于纯水和碱溶液,微溶于氨溶液,难溶于乙醇和甘油,不溶于丙酮,25 °C时在水中的溶解度为8.61 g/100 g,且溶解度随温度升高而大幅度升高,在20 ℃时的密度为2.34 g/cm³,熔点为368 ℃,沸点为400 °C;20 °C时的折射率为1.440。
化学性质
分解反应
氯酸钾是一种极其不稳定的物质,加热至368 ℃左右时开始熔化分解释放氧气,同时放出热量(氯酸盐具有分解时放热的特性)随着温度的增加,氧气不断放出,在温度到达610 ℃时会完全分解,将所有氧转换为氧气。整个反应可用如下反应方程式表示:


| 
| 图意 | 氧化物 | 有刺激性 | 对水生生物毒性很大 |
GHS分类:
H271:可能引起火灾或爆炸;强氧化剂[危险氧化液体;氧化性固体]
H302:吞咽有害[警告急性毒性,口服]
H332:吸入有害[警告急性毒性,吸入]
H411:对水生生物有毒,影响长期[对水生环境有害,长期危害]
毒性
氯酸钾的毒性如下表所示。
实验生物体 | 摄入路线 | 最低致死剂量 |
豚鼠 | 腹腔 | 1800 mg/kg |
大鼠 | 腹膜 | 1500 mg/kg |
狗 | 口腔 | 0.12 mg/kg |
人 | 口腔 | 1 mg/kg |
氯酸钾是强氧化剂进入人体后会使血液中的血红蛋白转化为高铁血红蛋白,从而导致血管内血管凝聚,引起血栓,导致死亡。
氯酸钾对肾小管有毒性,摄入氯酸钾可能会造成肾小管衰竭。
健康危害
氯酸钾燃烧会产生刺激性有毒烟雾。人吸入后会刺激鼻腔和喉咙,同时会刺激肺部和粘膜,出现咳嗽、窒息和意识丧失等症状。接触时刺激皮肤和眼睛时,眼睛可能会出现瘙痒、流泪和发红的症状,严重者可能会出现角膜损伤;皮肤可能会出现发红、起泡、起皮和瘙痒等症状,长时间接触会出现溃疡。摄入会导致腹痛、感到恶心、甚至感到虚脱。
储存方式
氯酸钾必须存放在干燥,且通风良好的场所。同时,存放处需避免阳光直射、远离火源和热源、可燃材料及会发生反应的材料——包括其他肥料、还原剂、金属粉末、任何腐蚀性材料和有机材料。
如果将氯酸钾与化肥、杀虫剂或其他化学物质一起储存,极易出现火灾或爆炸。
防治措施
健康相关
为了避免吸入、皮肤渗透和摄入氯酸钾对人体造成的慢性影响:
1.在需要使用氯酸钾的工作中需要保持一个良好的通风环境;
2.工作时做好个人防护需要佩戴安全眼镜或护目镜、聚氯乙烯手套、NIOSH/MSHA批准的防尘口罩/呼吸器、防透水靴子和工作服。(避免使用布或皮革材质的防护装备,以免与氯酸钾发生反应产生意外危险);
3.在进行有关氯酸钾的工作后,需要对手和脸部进行清洗。
消防相关
氯酸钾是一种强氧化剂和一种非常活泼的物质,在加热和与其他还原性物质、酸、有机物混合时可能会发生爆炸危险。
在处理有关氯酸钾的火灾事故时,需要注意佩戴正压自给式呼吸器(SCBA)和穿着特定防护服避免氯酸钾释放出的有毒氯化物烟雾对身体的损害。
在处理有关氯酸钾的火灾事故时,需要使用水灭火,不要使用干粉灭火器或泡沫灭火器。因为CO₂或哈龙可对火灾的控制效果低。
急救措施
1.若眼睛不小心接触氯酸钾,应立即分开眼睑用流动清水或生理盐水冲洗15分钟;若有不适感,请立即送往医院就医。
2.若皮肤不小心接触氯酸钾,应立即用肥皂和水冲洗接触处,若有不适感,请立即送往医院就医。
3.若不小心吸入氯酸钾,应立即将人移至新鲜空气处,必要时通过需要非循环呼吸面罩帮助患者辅助通气或提供人工呼吸。
4.若不小心摄入氯酸钾,需立即通过饮用肥皂或稀释盐水诱导呕吐并立即前往医院就医。