发现历史
15世纪,德国的炼金术士瓦伦丁(Valentin)把食盐与绿矾(即七水硫酸亚铁,FeSO₄·7H₂O)一起加热,得到了“氢氯酸”(spirit of salt)。
17世纪,德国药剂师格劳勃(Glauber)通过加热氯化钠和硫酸制取硫酸钠,并用水吸收逸出的刺激性气体得到盐酸。这是最古老的实验室制取盐酸的方法,目前人们仍然会通过此方式制取少量氯化氢气体。
1790年,英国化学家戴维(Davy)证明氢元素和氯元素组成了氯化氢。在电解食盐水时,他发现自己得到的产物除了氢氧化钠溶液,还有氢气和氯气。在同一年,法国化学家勒布朗(Leblanc)探索出了生产碳酸钠的工艺。该方法的第一步需要将氯化钠与硫酸加热制备硫酸钠,此过程产生的副产物氯化氢气体会被直接排放到空气中。
1836年,英国的化学品制造商威廉·戈萨奇(William Gossage,1799-1877)采用填充焦炭的洗涤塔回收氯化氢,此举是为了减少氯化氢气体对环境的破坏。同年英国颁布了世界上首个针对环境保护的碱工业法规,限令各工厂必须回收生产中产生的副产物氯化氢气体,工业上开始大规模产出盐酸。那些过量的不能用于制备盐酸的氯化氢气体被氧化生成氯气,作为生产漂白粉的原料。
20世纪初,氯化氢合成工艺有了极大的进步,人们通过氯碱电解工艺可以制备高纯度的氯化氢气体。且随着人们对环境保护的日益重视,专门生产氯化氢的工艺已被逐步淘汰,人们开始从氯化过程(如乙烯生产氯乙烯)及焚烧含氯废物产生的气体中回收氯化氢气体以制取盐酸。
化学性质
和酸碱指示剂反应
盐酸是无机强酸,在紫色或蓝色石蕊试纸上滴盐酸,试纸会变成红色,在无色酚酞溶液中滴入盐酸,酚酞溶液不会变色,人们可以应用此性质鉴别酸和其他溶液。
和碱发生中和反应
盐酸能和NaOH、Mg(OH)₂、Al(OH)₃等碱反应:
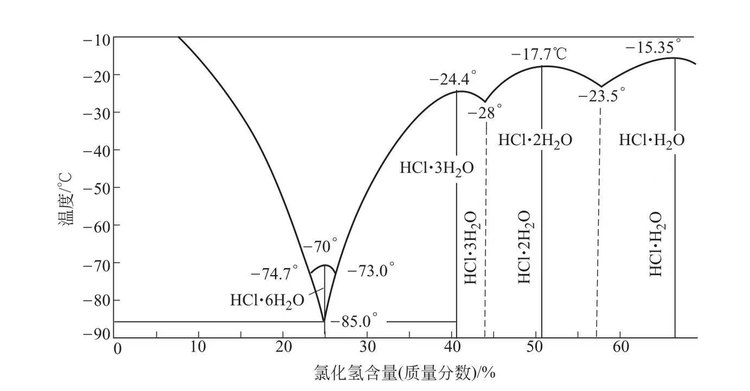
盐酸的恒沸点为108.5 ℃,下表是不同压力下的盐酸的恒沸组成。
压力/mmHg | 730 | 740 | 750 | 760 | 770 |
氯化氢质量分数/% | 20.314 | 20.290 | 20.266 | 20.242 | 20.218 |
应用领域
实验室应用
调节pH:盐酸能够中和碱液、调节溶液的pH值,具体应用:处理某些实验室废液时,可以使用盐酸调节pH使其达到排放标准;某些合成反应需要在一定的pH值下进行,可以使用盐酸进行调节,等等。
焰色反应:焰色反应可以鉴别金属离子,盐酸在焰色反应中可用来清洗铂棒避免其他离子对结果产生干扰。

酸碱滴定:盐酸可用于配置酸标准溶液。
稀有金属的湿法冶金
盐酸的反应能力强,因而可以浸出多种金属、金属氧化物以及部分硫化物,在湿法冶金中可用于浸出镍锍、钴渣等。以冶炼金属钨为例,将白钨矿和碳酸钠反应后得到的主要产物钨酸钠溶于水后,加盐酸酸化可以得到钨酸沉淀,能够将钨元素与其他杂质分离。
有机合成
例如,氯化氢和乙炔能在180 ℃-200 ℃、汞盐(如HgCl₂)催化的条件下发生加成反应,生成氯乙烯。

泄漏相关
盐酸泄漏后,人员应迅速撤离并隔离污染泄漏区。盐酸少量泄漏,可以用沙土或干石灰混合掩埋或使用大量水冲洗盐酸;盐酸大量泄漏,则需要挖坑或使用专用的容器收容,并将盐酸运送到专业的处理厂处理。
健康相关
GHS危险性类别:
项目 | 类别 |
加压气体 | 液化气体 |
皮肤腐蚀/刺激 | 1A |
急性吸入毒性 | 3 |
皮肤直接接触盐酸会被灼烧,长期接触可能会导致皮炎。
眼睛接触盐酸可能会导致视力下降或失明。
呼吸道吸入盐酸会产生刺激,可能会导致炎症和肺水肿。
口腔摄入盐酸会导致黏膜、食道和胃腐蚀,长期接触可能会腐蚀牙齿,以及引发消化系统疾病。
急救措施
盐酸接触眼睛,应立即使用清水清洗眼睛15钟,并且尽快就医。
盐酸接触皮肤,应立即用大量清水冲洗接触盐酸的皮肤15分钟,可以在皮肤上涂抹如肥皂水这样的弱碱性物质并及时就医。
呼吸道接触盐酸,立即转移至空气新鲜处,保持呼吸畅通并尽快就医。
运输相关
高纯盐酸腐蚀性极强,禁止和有毒、有害物品混运或混储,接触的人员必须穿戴好防护用具。
使用聚氯乙烯桶或陶瓷坛封装高纯盐酸时,注料口需要用螺栓盖盖住,并且要用耐酸材料封闭盖子,之后装入木箱,箱口要比注料口至少高2 cm,使用槽车及储罐进行包装时应衬胶并加密封盖。
环境相关
浓盐酸挥发性强,挥发在空气中会形成白雾,严重污染空气。
泄漏到土地上的盐酸会导致土壤酸化,使农作物绝产,严重影响耕种。盐酸泄漏到水域中,使水体pH急剧下降,对水生生物和地泥微生物造成致命危害。
工业废盐酸的处理
参照GB/T 32125-2021,工业废盐酸需要根据其特点,选择合适的方式对盐酸进行回收利用或达到排放标准后排放,常见的处理方式有蒸发结晶、硫酸置换、焙烧、制备四氧化三铁等。